Exubera pentru tratamentul diabetului
Nume de marcă: Exubera
Denumire generică: insulină umană
Forma de dozare: pulbere de inhalare
Cuprins:
Descriere
Farmacologie clinică
Studii clinice
Indicații și utilizare
Contraindicații
Avertizări
Măsuri de precauție
Interacțiunile medicamentoase
Reactii adverse
Supradozarea
Dozaj si administrare
Cât este furnizat
Exubera, insulină umană [origine ADNc] Informații despre pacient (în engleză simplă)
Descriere
Exubera® constă din blistere care conțin pulbere de inhalare de insulină umană, care sunt administrate cu Exubera® Inhalator. Blisterele Exubera conțin insulină umană produsă prin tehnologia ADN recombinantă care utilizează o tulpină de laborator nepatogenă de Escherichia coli (K12). Chimic, insulina umană are formula empirică C257H383N65O77S6 și o masă moleculară de 5808. Insulina umană are următoarea secvență de aminoacizi primari:
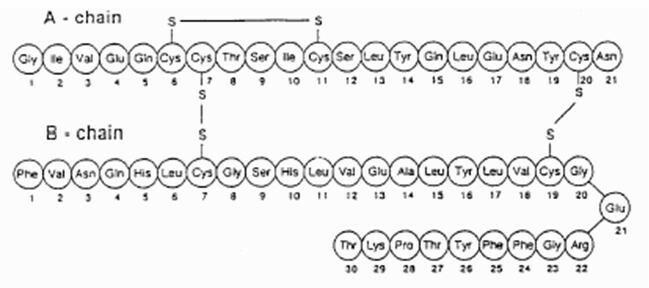
Exubera (insulină umană [origine ADNc]) Pulberea de inhalare este o pulbere de culoare albă până la albă într-o blister doză unitară (masă de umplere, vezi Tabelul 1). Fiecare blister de doză unitară de Exubera conține o doză de insulină de 1 mg sau 3 mg (vezi tabelul 1) în a formulare omogenă de pulbere care conține citrat de sodiu (dihidrat), manitol, glicină și sodiu hidroxid. După ce un blister Exubera este introdus în inhalator, pacientul pompează mânerul inhalatorului și apoi apasă un buton, făcând să fie străpuns blisterul. Pulberea de inhalare a insulinei este apoi dispersată în cameră, permițând pacientului să inhaleze pulberea aerosolizată.
În condiții de testare in vitro standardizate, Exubera furnizează o doză specifică de insulină emisă de către dispozitivul bucal al inhalatorului (vezi Tabelul 1). O fracțiune din masa totală a particulelor este emisă sub formă de particule fine, capabile să ajungă la plămânul profund. Până la 45% din conținutul de 1 mg de blister și până la 25% din conținutul de 3 mg blister pot fi păstrate în blister.
Tabelul 1: Nomenclatura dozei și informații
| Masa de umplere (mg pulbere) |
Doza nominală (mg insulină) |
Doza emisă*,†(mg insulină) |
Doza cu particule finec,†(mg insulină) |
|---|---|---|---|
| |||
| 1.7 | 1.0 | 0.53 | 0.4 |
| 5.1 | 3.0 | 2.03 | 1.0 |
Cantitatea reală de insulină livrată plămânului va depinde de factori individuali ai pacientului, cum ar fi profilul fluxului inspirator. In vitro, valorile de aerosoli emise nu sunt afectate la debite peste 10 L / min.
top
Farmacologie clinică
Mecanism de acțiune
Activitatea principală a insulinei este reglarea metabolismului glucozei. Insulina scade concentrațiile de glucoză din sânge prin stimularea absorbției periferice a glucozei de către mușchii și grăsimile scheletice și prin inhibarea producției de glucoză hepatică. Insulina inhibă lipoliza în adipocit, inhibă proteoliza și îmbunătățește sinteza proteinelor.
Farmacocinetica
Absorbţie
Exubera livrează insulină prin inhalare orală. Insulina este absorbită la fel de rapid ca analogii cu insulină cu acțiune rapidă administrată subcutanat și mai rapid decât administrată subcutanat insulină umană regulată la subiecți sănătoși și la pacienți cu diabet de tip 1 sau de tip 2 (vezi Figura 1).
Figura 1: Modificări medii ale concentrațiilor serice de insulină liberă (µU / ml) la pacienții cu diabet zaharat de tip 2 Administrarea de doze unice de insulină inhalată de la Exubera (6 mg) și insulină umană regulată subcutanată (18U)
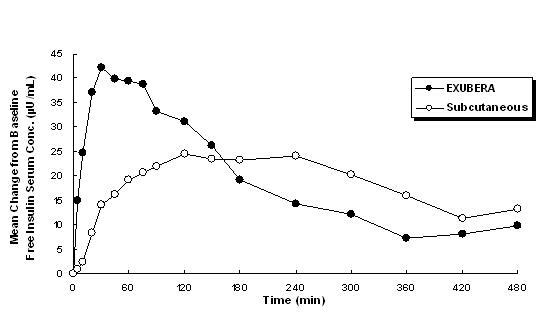
În studiile clinice la pacienții cu diabet zaharat tip 1 și 2, după inhalarea de Exubera, insulina serică a atins concentrația maximă mai repede decât după injecția subcutanată de insulină umană obișnuită, 49 de minute (interval de 30 până la 90 de minute) comparativ cu 105 minute (interval de 60 până la 240 de minute), respectiv.
În studiile clinice, absorbția insulinei umane regulate subcutanate a scăzut odată cu creșterea indicelui de masă corporală al pacientului (IMC). Cu toate acestea, absorbția insulinei în urma inhalării Exubera a fost independentă de IMC.
Într-un studiu la subiecți sănătoși, expunerea sistemică la insulină (ASC și Cmax) după administrarea de Exubera a crescut cu doza pe o gamă de 1 până la 6 mg atunci când se administrează sub formă de combinații de 1 și 3 mg blistere.
Într-un studiu în care forma de dozare de trei blistere de 1 mg a fost comparată cu un blister de 3 mg, Cmax și AUC după administrarea trei blistere de 1 mg au fost cu aproximativ 30% și respectiv cu 40% mai mari decât cea după administrarea unui blister de 3 mg (vezi DOZAJ SI ADMINISTRARE).
Distribuție și eliminare
Deoarece insulina umană recombinantă este identică cu insulina endogenă, se preconizează că distribuția și eliminarea sistemică sunt aceleași. Cu toate acestea, acest lucru nu a fost confirmat pentru Exubera.
Farmacodinamica
Exubera, ca și analogii cu insulină cu acțiune rapidă administrată subcutanat, are un debut mai rapid al activității de scădere a glucozei decât insulina umană obișnuită administrată subcutanat. La voluntarii sănătoși, durata activității de scădere a glucozei pentru Exubera a fost comparabilă cu cea subcutanată administrată insulină umană regulată și mai lungă decât analogii cu insulină cu acțiune rapidă administrată subcutanat (vezi Figura 2).
Figura 2. Rata medie de perfuzie a glucozei (GIR) Normalizată la GIRmax pentru fiecare subiect de tratament comparativ cu timpul la voluntarii sănătoși
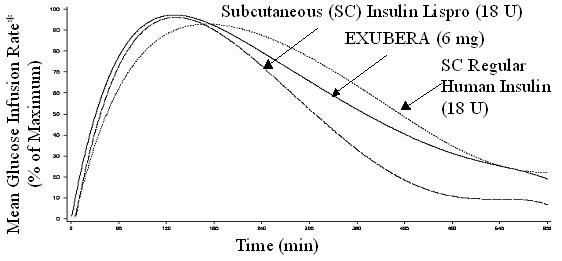
* Determinată ca cantitate de glucoză perfuzată pentru a menține concentrații constante de glucoză în plasmă, normalizată la valori maxime (procent din valorile maxime); indicativ al activității insulinei.
Când Exubera este inhalat, debutul activității de scădere a glucozei la voluntari sănătoși apare în 10-20 de minute. Efectul maxim asupra scăderii glucozei se exercită la aproximativ 2 ore după inhalare. Durata activității de scădere a glucozei este de aproximativ 6 ore.
La pacienții cu diabet de tip 1 sau de tip 2, Exubera are un efect mai mare de reducere a glucozei în primele două ore după administrare, în comparație cu insulina umană obișnuită administrată subcutanat.
Variabilitatea intra-subiect a activității de scădere a glucozei din Exubera este în general comparabilă cu cea a insulinei umane administrate subcutanat la pacienții cu diabet zaharat tip 1 și 2.
Populații speciale
Pacienți pediatri
La copii (6-11 ani) și adolescenți (12-17 ani) cu diabet zaharat tip 1, perioada de concentrație de insulină maximă pentru Exubera a fost de obținut mai repede decât pentru insulina umană regulată subcutanată, care este în concordanță cu observațiile la pacienții adulți cu tipul 1 Diabet.
Pacienți geriatrici
Nu există diferențe aparente în ceea ce privește proprietățile farmacocinetice ale Exubera atunci când se compară pacienții cu vârsta peste 65 de ani și pacienții adulți tineri.
Sex
La subiecții cu și fără diabet, nu au fost observate diferențe aparente în proprietățile farmacocinetice ale Exubera între bărbați și femei.
Cursă
Un studiu a fost realizat la 25 de subiecți sănătoși caucazieni și non-diabetici japonezi pentru a compara aceste proprietățile farmacocinetice și farmacodinamice ale Exubera, comparativ cu injecția subcutanată a omului obișnuit insulină. Proprietățile farmacocinetice și farmacodinamice ale Exubera au fost comparabile între cele două populații.
obezitatea
Absorbția de Exubera este independentă de IMC al pacientului.
Insuficiență renală
Efectul insuficienței renale asupra farmacocineticii Exubera nu a fost studiat. Monitorizarea atentă a glucozei și ajustarea dozei de insulină pot fi necesare la pacienții cu disfuncție renală (vezi PRECAUȚII, Insuficiență renală).
Deficiență hepatică
Efectul insuficienței hepatice asupra farmacocineticii Exubera nu a fost studiat. Monitorizarea atentă a glucozei și ajustarea dozei de insulină pot fi necesare la pacienții cu disfuncție hepatică (vezi PRECAUȚII).
graviditate
Absorbția Exubera la pacienții gravide cu diabet zaharat de tip 2 gestațional și pre-gestațional a fost în concordanță cu cea la pacienții care nu sunt gravide cu diabet zaharat de tip 2 (vezi PRECAUȚII).
Fumat
La fumători, expunerea sistemică la insulină pentru Exubera este de 2 până la 5 ori mai mare decât la nefumători. Exubera este contraindicat la pacienții care fumează sau care au întrerupt fumatul cu mai puțin de 6 luni înainte de începerea tratamentului cu Exubera. Dacă un pacient începe sau reia fumatul, Exubera trebuie întrerupt imediat din cauza riscului crescut de hipoglicemie și trebuie utilizat un tratament alternativ (vezi CONTRAINDICAȚII).
În studiile clinice efectuate pe Exubera la 123 de pacienți (dintre care 69 erau fumători), fumătorii au prezentat un debut mai rapid al acțiunii de reducere a glucozei, efect maxim mai mare și un efect mai mare de reducere a glucozei (în special în primele 2-3 ore după administrare), comparativ cu nefumătorii.
Fum de tigara pasiva
Spre deosebire de creșterea expunerii la insulină în urma fumatului activ, când Exubera a fost administrat la 30 de voluntari sănătoși nefumători după 2 ore de expunere la fum de țigară pasivă într-un cadru experimental controlat, ASC de insulină și Cmax au fost reduse cu aproximativ 20% și 30%, respectiv. Farmacocinetica Exubera nu a fost studiată la nefumătorii care sunt expuși cronic la fumul de țigară pasivă.
Pacienți cu boli pulmonare subiacente
Nu este recomandată utilizarea Exubera la pacienții cu boală pulmonară de bază, precum astmul sau BPOC, deoarece nu a fost stabilită siguranța și eficacitatea Exubera la această populație (vezi AVERTIZĂRI). Utilizarea Exubera este contraindicată la pacienții cu boală pulmonară instabilă sau slab controlată, din cauza laturii variații ale funcției pulmonare care ar putea afecta absorbția Exubera și crește riscul de hipoglicemie sau hiperglicemie (vezi CONTRAINDICAȚII).
Într-un studiu farmacocinetic la 24 de subiecți non-diabetici cu astm ușor, absorbția insulinei după administrarea de Exubera, în absența tratamentului cu bronhodilatator, a fost cu aproximativ 20% mai mic decât absorbția observată la subiecți fără astm. Cu toate acestea, într-un studiu efectuat la 24 de subiecți non-diabetici cu boală pulmonară obstructivă cronică (BPOC), sistemul este expunerea după administrarea de Exubera a fost de aproximativ două ori mai mare decât cea la subiecții normali fără BPOC (vezi PRECAUȚII).
Administrarea de albuterol cu 30 de minute înainte de administrarea de Exubera la subiecți non-diabetici cu astm ușor (n = 36) și moderat astmul (n = 31) a dus la o creștere medie a ASC a insulinei și a Cmax între 25 și 50% comparativ cu administrarea de Exubera singur (vezi PRECAUȚII).
top
Studii clinice
Siguranța și eficacitatea Exubera au fost studiate la aproximativ 2500 de pacienți adulți cu diabet zaharat tip 1 și 2. Parametrul de eficacitate primar pentru majoritatea studiilor a fost controlul glicemic, măsurat prin reducerea de la nivelul inițial al hemoglobinei A1c (HbA1c).
Diabetul de tip 1
A fost efectuat un studiu de control activ (randomized, open-label), de 24 de săptămâni, la pacienții cu diabet zaharat tip 1 pentru a evalua siguranța și eficacitatea Exubera a fost administrată înainte de masă de trei ori pe zi (TID) cu o singură injecție nocturnă de Humulin® U Ultralente® (suspensie de zinc extinsă pentru insulină umană) (n = 136). Tratamentul comparativ a fost insulină umană regulată subcutanată administrată de două ori pe zi (BID) (dinaintea micului dejun și pre-cină) cu injecție BID de insulină umană NPH (suspensie de insulină umană izofan) (n = 132). În acest studiu, vârsta medie a fost de 38,2 ani (interval: 20-64) și 52% dintre subiecți au fost bărbați.
Un al doilea studiu de 24 de săptămâni, randomizat, deschis, cu control activ (Studiul B) a fost realizat la pacienții cu diabet zaharat tip 1 pentru a evalua siguranța și eficacitatea Exubera (n = 103) în comparație cu insulina umană regulată subcutanată (n = 103) când a fost administrată TID înainte de mese. În ambele brațe de tratament, insulina umană NPH a fost administrată BID (dimineața și la culcare) sub formă de insulină bazală. În acest studiu, vârsta medie a fost de 38,4 ani (interval: 19-65) și 54% dintre subiecți au fost bărbați.
În fiecare studiu, reducerea HbA1c și ratele de hipoglicemie au fost comparabile pentru cele două grupuri de tratament. Pacienții tratați cu exubera au avut o reducere mai mare a glucozei plasmatice în condiții de repaus decât pacienții din grupul comparator. Procentul de pacienți care ating un nivel de HbA1c <8% (pentru acțiunea de tratament a Asociației Americane pentru Diabet) Nivelul la momentul efectuării studiului) și un nivel de HbA1c <7% a fost comparabil între cele două grupuri de tratament. Rezultatele pentru studiile A și B sunt prezentate în tabelul 2.
Tabelul 2: Rezultatele a două studii de 24 de săptămâni, cu control activ, cu etichetă deschisă la pacienții cu diabet zaharat de tip 1 (studiile A și B)
| Studiul A | Studiul B | |||
|---|---|---|---|---|
| Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) | Exubera (TID) + NPH (BID) | SC R (TID) + NPH (BID) | |
| Marime de mostra | 136 | 132 | 103 | 103 |
| UL = Humulin® U Ultralente®; SC R = insulină umană regulată subcutanată | ||||
| ||||
| HbA1c (%) | ||||
| Media de bază | 7.9 | 8.0 | 7.8 | 7.8 |
| Adj. schimbare medie de la linia de bază | -0.2 | -0.4 | -0.3 | -0.2 |
| Exubera minus SC R* | 0.14 | -0.11 | ||
| IC 95% pentru diferența de tratament | (-0.03, 0.32) | (-0.30, 0.08) | ||
| Glucoză cu plasmă de post (mg / dL) | ||||
| Media de bază | 191 | 198 | 178 | 191 |
| Adj. schimbare medie de la linia de bază | -32 | -6 | -23 | 13 |
| Exubera minus SC R | -27 | -35 | ||
| IC 95% pentru diferența de tratament | (-47, -6) | (-58, -13) | ||
| Concentrația de glucoză post-prandială de 2 ore (mg / dL) | ||||
| Media de bază | 283 | 305 | 273 | 293 |
| Adj. schimbare medie de la linia de bază | -21 | 14 | -1 | -3 |
| Exubera minus SC R | -35 | 2 | ||
| IC 95% pentru diferența de tratament | (-61, -8) | (-29, 32) | ||
| Pacienții cu HbA la sfârșitul studiului1c < 8%†| 64.0% | 68.2% | 74.8% | 66.0% |
| Pacienții cu HbA la sfârșitul studiului1c < 7% | 16.9% | 19.7% | 28.2% | 30.1% |
| Greutate corporala | ||||
| Media de bază (kg) | 77.4 | 76.4 | 76.0 | 76.9 |
| Adj. modificarea medie de la valoarea de bază (kg) | 0.4 | 1.1 | 0.4 | 0.6 |
| Exubera minus SC R | -0.72 | -0.24 | ||
| IC 95% pentru diferența de tratament | (-1.48, 0.04) | (-1.07, 0.59) | ||
| Sfârșitul studiului doza zilnică de insulină | ||||
| Insulină cu acțiune scurtă | 13,4 mgc | 18.3 UI | 10,9 mgc | 25.7 UI |
| Insulina cu actiune indelungata | 26.4 UI | 37.1 UI | 31,5 UI | 31.9 UI |
Diabetul de tip 2
Monoterapie la pacienți care nu sunt controlate în mod optim cu dieta și tratamentul cu exerciții fizice
A fost efectuat un studiu de control activ (randomized, open-label), de 12 săptămâni, la pacienții cu diabet de tip 2, nu în mod optim controlat cu dieta și exercițiile fizice, evaluând siguranța și eficacitatea TID Exubera înainte de masă (n = 75) comparativ cu agent de sensibilizare la insulină. În acest studiu, vârsta medie a fost de 53,7 ani (interval: 28-80), 55% dintre subiecți au fost bărbați, iar indicele de masă corporală medie a fost de 32,3 kg / m2.
La 12 săptămâni, HbA1c nivelurile la pacienții tratați cu Exubera au scăzut cu 2,2% (SD = 1,0) de la valoarea inițială de 9,5% (SD = 1,1). Proporția pacienților tratați cu Exubera a ajuns la HbA la sfârșitul studiului1c nivelul de <8% a crescut la 82,7%. Proporția pacienților tratați cu Exubera a ajuns la HbA la sfârșitul studiului1c nivelul de
Monoterapie și terapie suplimentară la pacienții tratați anterior cu terapie cu agent oral
Un studiu de control activ (randomised, open-label), de 12 săptămâni, a fost realizat la pacienții cu tip 2 diabet care au primit tratament în prezent, dar au fost slab controlați, cu doi agenți orali (OA). OA inițiale includ un secretagog de insulină și metformină sau tiazolidinioneză. Pacienții au fost randomizați la unul dintre cele trei brațe: continuarea terapiei OA singure (n = 96), trecerea la monoterapie TID Exubera înainte de masă (n = 102) sau adăugarea TID Exubera înainte de masă la terapia OA continuată (n = 100). În acest studiu, vârsta medie a fost de 57,4 ani (interval: 33-80), 66% dintre subiecți au fost bărbați, iar indicele de masă corporală medie a fost de 30 kg / m2.
Monoterapia Exubera și Exubera în combinație cu terapia cu OA au fost superioare terapiei OA singure în reducerea HbA1c niveluri de la nivelul de bază. Ratele de hipoglicemie pentru cele două grupuri de tratament Exubera au fost puțin mai mari decât în lotul terapeutic OA. Comparativ cu terapia OA, procentul de pacienți care atinge un HbA1c nivel de <8% (pentru tratamentul Asociației americane pentru diabet zaharat Nivel de acțiune la momentul efectuării studiului) și un HbA1c nivelul de <7% a fost mai mare pentru pacienții tratați cu Exubera monoterapie și Exubera în asociere cu terapia OA. Pacienții din ambele grupuri de tratament Exubera au avut reduceri mai mari ale glucozei plasmatice în condiții de repaus decât pacienții tratați cu terapie OA. Rezultatele studiului D sunt prezentate în tabelul 3.
Tabelul 3: Rezultatele unui test de 12 săptămâni, cu control activ, cu etichetă deschisă, la pacienții cu diabet zaharat de tip 2, care nu sunt controlate în mod optim cu terapia dublă cu agent oral (studiu D)
| Studiul D | Monoterapie exubera | OAS* | Exubera + OAs |
|---|---|---|---|
| Marime de mostra | 102 | 96 | 100 |
| |||
| HbA1c (%) | |||
| Media de bază | 9.3 | 9.3 | 9.2 |
| Adj. schimbare medie de la linia de bază | -1.4 | -0.2 | -1.9 |
| Exubera grup minus OA-uri†| -1.18†,c, § | -1.67†, ¶, § | |
| IC 95% pentru diferența de tratament | (-1.41, -0.95) | (-1.90, -1.44) | |
| Glucoză cu plasmă de post (mg / dL) | |||
| Media de bază | 203 | 203 | 195 |
| Adj. schimbare medie de la linia de bază | -23 | 1 | -53 |
| Exubera grup minus OA-uri | -24c | -53 ¶ | |
| IC 95% pentru diferența de tratament | (-36, -11) | (-66, -41) | |
| Pacienții cu HbA la sfârșitul studiului1c < 8%# | 55.9% | 18.8% | 86.0% |
| Pacienții cu HbA la sfârșitul studiului1c < 7% | 16.7% | 1.0% | 32.0% |
| Greutate corporala | |||
| Media de bază (kg) | 89.5 | 88.0 | 88.6 |
| Adj. modificarea medie de la valoarea de bază (kg) | 2.8 | 0.0 | 2.7 |
| Exubera grup minus OA-uri | 2.80c | 2.75 ¶ | |
| IC 95% pentru diferența de tratament | (1.94, 3.65) | (1.89, 3.61) |
Un studiu de control activ (randomised, open-label), de 24 de săptămâni, a fost realizat la pacienții cu diabet zaharat de tip 2, care beneficiază în prezent de terapie cu sulfonilurea. Acest studiu a fost conceput pentru a evalua siguranța și eficacitatea adăugării de Exubera înainte de masă în continuare terapia cu sulfonilurea (n = 214) comparativ cu adăugarea metforminei dinaintea mesei la terapia cu sulfonilurea continuată (n = 196). Subiectele au fost stratificate în funcție de HbA1c în săptămâna -1. Au fost definite două straturi: un strat HbA1c scăzut (HbA)1c â ‰ ¥ 8% până la ‰ ¤9,5%) și un HbA ridicat1c strat (HbA)1c > 9,5 până la ‰ ¤12%).
Exubera în combinație cu sulfonilurea a fost superioară metforminei și sulfonilureei în reducerea valorilor HbA1c de la nivelul inițial din grupa stratului înalt. Exubera în combinație cu sulfonilurea a fost comparabilă cu metformină în combinație cu sulfonilurea în reducerea valorilor HbA1c de la nivelul inițial din grupa stratului scăzut. Rata de hipoglicemie a fost mai mare după adăugarea de Exubera la sulfonilurea decât după adăugarea de metformină la sulfoniluree. Procentul de pacienți care au atins valori HbA1c de 8% și 7% a fost comparabil între grupurile de tratament din ambele straturi, precum și reducerea glucozei plasmatice în condiții de repaus (vezi vezi Tabelul 4).
Un alt studiu de control activ (randomized, open-label), de 24 de săptămâni, a fost realizat la pacienții cu diabet zaharat de tip 2, care beneficiază în prezent de terapie cu metformină. Acest studiu a fost conceput pentru a evalua siguranța și eficacitatea adăugării de Exubera înainte de masă în continuare terapia cu metformin (n = 234) comparativ cu adăugarea glibenclamidei înainte de masă la terapia cu metformină continuă (n = 222). Subiecții din acest studiu au fost, de asemenea, stratificați la unul dintre cele două straturi, așa cum este definit în Studiul E.
Exubera în combinație cu metformin a fost superioară glibenclamidei și metforminei în reducerea HbA1c valori de la nivelul de bază și atingerea HbA țintă1c valori în grupul cu strat înalt. Exubera în asociere cu metformin a fost comparabilă cu glibenclamidă în combinație cu metformină în reducerea HbA1c valori de la nivelul de bază și atingerea HbA țintă1c valori în grupul stratului scăzut. Rata hipoglicemiei a fost ușor mai mare după adăugarea de Exubera la metformină decât după adăugarea de glibenclamidă la metformină. Reducerea glucozei plasmatice în condiții de repaus a fost comparabilă între grupurile de tratament (vezi Tabelul 4).
Tabelul 4: Rezultatele a două studii de 24 de săptămâni, cu control activ, cu etichetă deschisă, la pacienții cu diabet zaharat de tip 2, anterior la terapia cu agenți orali (studii E și F)
| Studiu E | Studiul F | |||||||
|---|---|---|---|---|---|---|---|---|
| Exubera + SU* | Întâlnit*+ SU* | Exubera + SU* | Întâlnit*+ SU* | Exubera + Met* | Gli* + Met* | Exubera + Met* | Gli* + Met* | |
| Strat înalt†| Strat redus†| Strat înalt†| Strat redus†| |||||
| Marime de mostra | 113 | 103 | 101 | 93 | 109 | 103 | 125 | 119 |
| ||||||||
| HbA1c (%) | ||||||||
| Media de bază | 10.5 | 10.6 | 8.8 | 8.8 | 10.4 | 10.6 | 8.6 | 8.7 |
| Adj. schimbare medie de la linia de bază | -2.2 | -1.8 | -1.9 | -1.9 | -2.2 | -1.9 | -1.8 | -1.9 |
| Exubera minus OAc | -0.38c, § | -0.07 | -0.37c, ¶ | 0.04 | ||||
| IC 95% pentru diferența de tratament | (-0.63, -0.14) | (-0.33, 0.19) | (-0.62, -0.12) | (-0.19, 0.27) | ||||
| Glucoză cu plasmă de post (mg / dL) | ||||||||
| Media de bază | 241 | 237 | 197 | 198 | 223 | 243 | 187 | 196 |
| Modificarea medie de la valoarea de bază | -46 | -47 | -48 | -52 | -42 | -40 | -46 | -49 |
| Exubera minus OA | 1 | 4 | -2 | 4 | ||||
| IC 95% pentru diferența de tratament | (-11, 12) | (-8, 16) | (-14, 10) | (-7, 15) | ||||
| Subiecții cu HbA la sfârșitul studiului1c < 8%# | 48.7% | 44.7% | 81.2% | 73.1% | 72.5% | 56.3% | 80.8% | 86.6% |
| Subiecții cu HbA la sfârșitul studiului1c < 7% | 20.4% | 14.6% | 30.7% | 32.3% | 33.9% | 17.5% | 40.0% | 42.9% |
| Greutate corporala | ||||||||
| Media de bază (kg) | 80.8 | 79.5 | 79.9 | 81.9 | 88.3 | 87.8 | 90.3 | 88.2 |
| Adj. modificarea medie de la valoarea de bază (kg) | 3.6 | -0.0 | 2.4 | -0.3 | 2.8 | 2.5 | 2.0 | 1.6 |
| Exubera minus OA | 3.60 | 2.67 | 0.26 | 0.38 | ||||
| IC 95% pentru diferența de tratament | (2.81, 4.39) | (1.84, 3.51) | (-0.70, 1.21) | (-0.52, 1.27) |
Utilizați la pacienții tratați anterior cu insulină subcutanată
A fost efectuat un studiu de control activ (randomized, open-label), de 24 de săptămâni, la pacienții tratați cu insulină cu tipul 2 diabet pentru a evalua siguranța și eficacitatea TID administrată înainte de masă Exubera cu o singură injecție nocturnă de Humulin® U Ultralente® (n = 146) comparativ cu insulina umană regulată subcutanată administrată BID (pre-micul dejun și înainte de cină) cu injecția BID de insulină umană NPH (n = 149). În acest studiu, vârsta medie a fost de 57,5 ani (interval: 23-80), 66% dintre subiecți au fost bărbați, iar indicele de masă corporală medie a fost de 30,3 kg / m2.
Reduceri de la valoarea inițială în HbA1c, la sută dintre pacienții care au ajuns la HbA1c nivel de <8% (pentru tratamentul Asociației americane pentru diabet zaharat Nivel de acțiune la momentul efectuării studiului) și un HbA1c nivelul de <7%, precum și ratele de hipoglicemie, au fost similare între grupurile de tratament. Pacienții tratați cu exubera au avut o reducere mai mare a glucozei plasmatice în condiții de repaus decât pacienții din grupul comparator. Rezultatele studiului G sunt prezentate în tabelul 5.
Tabelul 5: Rezultatele unui test de 24 de săptămâni, cu control activ, cu etichetă deschisă, la pacienții cu diabet zaharat de tip 2 Tratat anterior cu insulină subcutanată (Studiul G)
| Studiul G | Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) |
|---|---|---|
| Marime de mostra | 146 | 149 |
| UL = Humulin® U Ultralente®; SC R = insulină umană regulată subcutanată | ||
| ||
| HbA1c (%) | ||
| Media de bază | 8.1 | 8.2 |
| Adj. schimbare medie de la linia de bază | -0.7 | -0.6 |
| Exubera minus SC R* | -0.07 | |
| IC 95% pentru diferența de tratament | (-0.31, 0.17) | |
| Glucoză cu plasmă de post (mg / dL) | ||
| Media de bază | 152 | 159 |
| Adj. schimbare medie de la linia de bază | -22 | -6 |
| Exubera minus SC R | -16.36 | |
| IC 95% pentru diferența de tratament | (-27.09, -5.36) | |
| Pacienții cu HbA la sfârșitul studiului1c < 8%†| 76.0% | 69.1% |
| Pacienții cu HbA la sfârșitul studiului1c < 7% | 45.2% | 32.2% |
| Greutate corporala | ||
| Media de bază (kg) | 90.6 | 89.0 |
| Adj. modificarea medie de la valoarea de bază (kg) | 0.1 | 1.3 |
| Exubera minus SC R | -1.28 | |
| IC 95% pentru diferența de tratament | (-1.96, -0.60) | |
| Sfârșitul studiului doza zilnică de insulină | ||
| Insulină cu acțiune scurtă | 16,6 mgc | 25,5 UI |
| Insulina cu actiune indelungata | 37,9 UI | 52,3 UI |
top
Indicații și utilizare
Exubera este indicat pentru tratamentul pacienților adulți cu diabet zaharat pentru controlul hiperglicemiei. Exubera are o acțiune similară cu analogii cu insulină cu acțiune rapidă și are o activitate de scădere a glucozei, comparabilă cu insulina umană obișnuită administrată subcutanat. La pacienții cu diabet zaharat tip 1, Exubera trebuie utilizat în regimuri care includ o insulină cu acțiune mai lungă. La pacienții cu diabet zaharat tip 2, Exubera poate fi utilizat ca monoterapie sau în combinație cu agenți orali sau insuline cu acțiune mai lungă.
top
Contraindicații
Exubera este contraindicată la pacienții hipersensibili la Exubera sau la unul dintre excipienții săi.
Exubera este contraindicat la pacienții care fumează sau care au întrerupt fumatul cu mai puțin de 6 luni înainte de începerea tratamentului cu Exubera. Dacă un pacient începe sau reia fumatul, Exubera trebuie întrerupt imediat din cauza riscului crescut de hipoglicemie și trebuie utilizat un tratament alternativ (vezi FARMACOLOGIE CLINICĂ, Populații speciale, fumat). Siguranța și eficacitatea Exubera la pacienții care fumează nu au fost stabilite.
Exubera este contraindicată la pacienții cu boală pulmonară instabilă sau slab controlată, din cauza variațiilor mari în funcție pulmonară care ar putea afecta absorbția Exubera și crește riscul de hipoglicemie sau hiperglicemie.
top
Avertizări
Exubera diferă de insulina umană obișnuită prin debutul rapid al acțiunii. Când se utilizează ca insulină de masă, doza de Exubera trebuie administrată în decurs de 10 minute înainte de masă.
Hipoglicemia este cel mai frecvent raportat advers al terapiei cu insulină, inclusiv Exubera. Momentul hipoglicemiei poate diferi de la diferite formulări de insulină.
Pacienții cu diabet zaharat tip 1 necesită, de asemenea, o insulină cu acțiune mai lungă pentru a menține un control adecvat al glucozei.
Orice schimbare de insulină trebuie făcută cu precauție și numai sub supraveghere medicală. Modificările de rezistență la insulină, producătorul, tipul (de exemplu, regulat, NPH, analogi) sau specii (animal, uman) pot duce la necesitatea unei modificări a dozelor. Poate fi necesar să fie ajustat tratamentul antidiabetic oral concomitent.
Monitorizarea glucozei este recomandată tuturor pacienților cu diabet zaharat.
Din cauza efectului Exubera asupra funcției pulmonare, toți pacienții ar trebui să aibă evaluarea funcției pulmonare înainte de inițierea terapiei cu Exubera (vezi PRECAUȚII: Funcția pulmonară).
Nu este recomandată utilizarea Exubera la pacienții cu boală pulmonară de bază, precum astmul sau BPOC, deoarece nu a fost stabilită siguranța și eficacitatea Exubera la această populație (vezi PRECAUȚII: Boala pulmonară de bază).
În studiile clinice cu Exubera, au existat 6 cazuri recent diagnosticate de malignități pulmonare primare la pacienții tratați cu Exubera și 1 caz nou diagnosticat în rândul pacienților tratați prin comparatie. De asemenea, a existat un raport post-comercializare a unei malignități pulmonare primare la un pacient tratat cu Exubera. În studiile clinice controlate cu Exubera, incidența cancerului pulmonar primar nou la 100 de pacienți ani de expunere la medicament a fost de 0,13 (5 cazuri peste 3900 ani-pacient) pentru pacienții tratați cu Exubera și 0,02 (1 caz peste 4100 ani-pacient) pentru pacienții tratați comparativ. Au fost prea puține cazuri pentru a determina dacă apariția acestor evenimente este legată de Exubera. Toți pacienții care au fost diagnosticați cu cancer pulmonar au avut antecedente de fumat țigară.
top
Măsuri de precauție
General
La fel ca în cazul tuturor preparatelor de insulină, cursul timpului de acțiune Exubera poate varia la diferiți indivizi sau în momente diferite la același individ. Reglarea dozei de insulină poate fi necesară dacă pacienții își schimbă activitatea fizică sau planul lor obișnuit de masă. Cerințele de insulină pot fi modificate în condiții intercurente, cum ar fi boli, tulburări emoționale sau stres.
hipoglicemia
Ca și în cazul tuturor preparatelor de insulină, reacțiile hipoglicemice pot fi asociate cu administrarea de Exubera. Modificările rapide ale concentrațiilor serice de glucoză pot induce simptome similare hipoglicemiei la persoanele cu diabet, indiferent de valoarea glucozei. Simptomele de avertizare timpurie a hipoglicemiei pot fi diferite sau mai puțin pronunțate în anumite afecțiuni, cum ar fi lungul durata diabetului, a bolilor nervilor diabetici, utilizarea de medicamente precum beta-blocante sau controlul intens al diabetului (vedea PRECAUȚII: Interacțiuni medicamentoase). Astfel de situații pot duce la hipoglicemie severă (și, posibil, la pierderea cunoștinței) înainte de conștientizarea pacienților despre hipoglicemie.
Insuficiență renală
Nu s-au efectuat studii la pacienți cu insuficiență renală. La fel ca în cazul altor preparate de insulină, cerințele de doză pentru Exubera pot fi reduse la pacienții cu insuficiență renală (vezi FARMACOLOGIE CLINICĂ, Populații speciale).
Deficiență hepatică
Nu s-au efectuat studii la pacienți cu insuficiență hepatică. Ca și în cazul altor preparate de insulină, necesitățile de doză pentru Exubera pot fi reduse la pacienții cu insuficiență hepatică (vezi FARMACOLOGIE CLINICĂ, Populații speciale).
Alergie
Alergie sistemică
În studiile clinice, incidența generală a reacțiilor alergice la pacienții tratați cu Exubera a fost similară la cea la pacienții care utilizează regimuri subcutanate cu insulină umană regulată.
La fel ca în cazul altor preparate de insulină, poate apărea alergie generală rară, dar potențial gravă, care poate provoca erupții cutanate (inclusiv prurit) pe întreg corpul, respirație, respirație șuierătoare, reducerea tensiunii arteriale, puls rapid sau transpiraţie. Cazurile severe de alergie generalizată, inclusiv reacții anafilactice, pot pune viața în pericol. Dacă astfel de reacții apar de la Exubera, Exubera trebuie oprită și luate în considerare terapii alternative.
Producția de anticorpi
Anticorpii de insulină se pot dezvolta în timpul tratamentului cu toate preparatele de insulină, inclusiv Exubera. În studiile clinice ale Exubera, unde comparatorul a fost insulină subcutanată, creșterea nivelului de anticorpi pentru insulină (așa cum se reflectă în testele de activitate de legare la insulină) au fost semnificativ mai mari pentru pacienții care au primit Exubera decât pentru pacienții care au primit insulină subcutanată numai. Nu au fost identificate consecințe clinice ale acestor anticorpi în perioada studiilor clinice ale Exubera; cu toate acestea, nu se cunoaște semnificația clinică pe termen lung a acestei creșteri a formării de anticorpi.
Respirator
Funcția pulmonară
În studiile clinice cu o durată de până la doi ani, pacienții tratați cu Exubera au demonstrat o scădere mai mare a funcției pulmonare, în special volumul expirator forțat într-o secundă (FEV1) și capacitatea de difuzie a monoxidului de carbon (DLCO), decât tratarea comparativă pacienți. Diferența medie a grupului de tratament în funcția pulmonară care favorizează grupul comparativ a fost remarcată în cadrul primele câteva săptămâni de tratament cu Exubera și nu s-au modificat în perioada de tratament de doi ani (Vedea REACTII ADVERSE: Funcția pulmonară).
În timpul studiilor clinice controlate, pacienții individuali au înregistrat scăderi notabile ale funcției pulmonare în ambele grupuri de tratament. O scădere de la valoarea inițială a FEV1 de 20% la ultima observație a avut loc la 1,5% dintre pacienții tratați cu Exubera și 1,3% dintre pacienții tratați prin comparatie. O scădere din DL-ul de bazăCO 20% la ultima observație au avut loc la 5,1% dintre pacienții tratați cu Exubera și 3,6% dintre pacienții tratați comparativ.
Din cauza efectului Exubera asupra funcției pulmonare, toți pacienții ar trebui să aibă evaluat spirometria (FEV1) înainte de inițierea terapiei cu Exubera. Evaluarea DLCO ar trebui luat în considerare. Eficacitatea și siguranța Exubera la pacienții cu FEV inițial1 sau DLCO <70% preconizate nu au fost stabilite, iar utilizarea Exubera în această populație nu este recomandată.
Evaluarea funcției pulmonare (de exemplu, spirometrie) este recomandată după primele 6 luni de terapie și, ulterior, ulterior, chiar și în absența simptomelor pulmonare. La pacienții cu un declin de 20% în FEV1 de la nivelul inițial, testele funcției pulmonare trebuie repetate. Dacă se confirmă scăderea de 20% față de valoarea de referință FEV1, Exubera trebuie întreruptă. Prezența simptomelor pulmonare și scăderi mai mici ale funcției pulmonare pot necesita monitorizarea mai frecventă a funcției pulmonare și luarea în considerare a întreruperii Exubera.
Boala pulmonară de bază
Nu este recomandată utilizarea Exubera la pacienții cu boli pulmonare subiacente, precum astmul sau BPOC, deoarece nu a fost stabilită eficacitatea și siguranța Exubera la această populație.
Spasm bronșic
Bronhospasmul a fost foarte rar raportat la pacienții care au luat Exubera. Pacienții care se confruntă cu o astfel de reacție ar trebui să întrerupă Exubera și să solicite imediat evaluarea medicală. Re-administrarea de Exubera necesită o evaluare atentă a riscului și ar trebui făcută doar sub monitorizare medicală atentă, cu dotări clinice adecvate disponibile.
Boala respiratorie intercurentă
Exubera a fost administrat pacienților cu afecțiuni respiratorii intercurente (de exemplu, bronșită, infecții ale tractului respirator superior, rinită) în timpul studiilor clinice. La pacienții care se confruntă cu aceste afecțiuni, 3-4% au întrerupt temporar terapia cu Exubera. Nu a existat niciun risc crescut de hipoglicemie sau control glicemic agravat observat la pacienții tratați cu Exubera în comparație cu pacienții tratați cu insulină subcutanată. În timpul bolilor respiratorii intercurente, poate fi necesară o monitorizare atentă a concentrațiilor de glucoză din sânge și ajustarea dozei.
Informații pentru pacienți
Pacienții trebuie instruiți cu privire la procedurile de auto-gestionare, inclusiv monitorizarea glucozei; tehnica corespunzătoare de inhalare Exubera; și managementul hipoglicemiei și hiperglicemiei. Pacienții trebuie instruiți cu privire la manipularea situațiilor speciale, cum ar fi afecțiuni intercurente (boală, stres sau emoțional tulburări), o doză de insulină inadecvată sau sărită, administrarea inadvertentă a unei doze crescute de insulină, aportul inadecvat de alimente sau mâncarea sărită
Pacienții trebuie informați că în studiile clinice, tratamentul cu Exubera a fost asociat cu scăderi medii, neprogresive, ale funcției pulmonare, în raport cu tratamentele comparative. Datorită efectului Exubera asupra funcției pulmonare, se recomandă testele funcției pulmonare înainte de inițierea tratamentului cu Exubera. După inițierea terapiei, se recomandă teste periodice ale funcției pulmonare (vezi PRECAUȚII Funcția respiratorie, pulmonară).
Pacienții trebuie să-și informeze medicul dacă au antecedente de boli pulmonare, deoarece nu se recomandă utilizarea Exubera în pacienți cu boală pulmonară de bază (de exemplu, astm sau BPOC) și este contraindicat la pacienții cu plămân slab controlat boală.
Femeile cu diabet trebuie sfătuite să informeze medicul dacă sunt însărcinate sau au în vedere sarcina.
top
Interacțiunile medicamentoase
O serie de substanțe afectează metabolismul glucozei și pot necesita o ajustare a dozei de insulină și o monitorizare îndeaproape atentă.
Următoarele sunt exemple de substanțe care pot reduce efectul de scădere a glucozei din sânge a insulinei care poate duce la hiperglicemie: corticosteroizi, danazol, diazoxid, diuretice, agenți simpatomimetici (de exemplu, epinefrină, albuterol, terbutalină), glucagon, izoniazid, derivați de fenotiazină, somatropină, hormoni tiroidieni, estrogeni, progestogeni (de exemplu, în contraceptive orale), inhibitori de protează și medicamente antipsihotice atipice (de exemplu, olanzapină și clozapină).
Următoarele sunt exemple de substanțe care pot crește efectul de scădere a glucozei din sânge a insulinei și susceptibilitatea la hipoglicemie: oral produse antidiabetice, inhibitori ACE, disopiramidă, fibrați, fluoxetină, inhibitori MAO, pentoxifilină, propoxifen, salicilați și sulfonamidă antibiotice.
Beta-blocante, clonidină, săruri de litiu și alcool pot crește sau reduce efectul de scădere a glucozei din sânge a insulinei. Pentamidina poate provoca hipoglicemie, care poate fi uneori urmată de hiperglicemie.
În plus, sub influența medicamentelor simpatolitice cum ar fi beta-blocante, clonidină, guanetidină și reserpină, semnele și simptomele hipoglicemiei pot fi reduse sau absente.
Bronhodilatatoarele și alte produse inhalate pot modifica absorbția insulinei umane inhalate (vezi FARMACOLOGIE CLINICĂ, Populații speciale). Este recomandată sincronizarea constantă a dozei de bronhodilatatoare în raport cu administrarea Exubera, monitorizarea atentă a concentrațiilor de glucoză din sânge și titrarea dozei, după caz.
Carcinogeneza, mutageneza, afectarea fertilitatii
Nu s-au efectuat studii de carcinogenitate de doi ani la animale. Insulina nu a fost mutagenă la testul de mutație inversă bacteriană Ames în prezența și absența activării metabolice.
La șobolanii Sprague-Dawley, un studiu de toxicitate în doză repetată de 6 luni a fost realizat cu pulbere de inhalare cu insulină în doze de până la 5,8 mg / kg / zi (comparativ cu clinic doza inițială de 0,15 mg / kg / zi, doza mare de șobolan a fost de 39 ori sau de 8,3 ori doza clinică, bazată fie pe o comparație de mg / kg, fie pe o comparație de suprafață corporală mg / m2). La maimuțele Cynomolgus, a fost efectuat un studiu de toxicitate în doză repetată de 6 luni cu insulină inhalată în doze de până la 0,64 mg / kg / zi. Comparativ cu doza de început clinică de 0,15 mg / kg / zi, doza mare de maimuță a fost de 4,3 ori 1,4 ori doza clinică, bazată fie pe o comparație de mg / kg, fie pe o suprafață corporală de mg / m2. Acestea au fost doze maxime tolerate bazate pe hipoglicemie.
În comparație cu animalele de control, nu au existat efecte adverse legate de tratament la nici o specie asupra funcției pulmonare, morfologiei brute sau microscopice a tractului respirator sau a ganglionilor bronșici. În mod similar, nu a existat niciun efect asupra indicilor de proliferare celulară în zona alveolară sau bronhiolară a plămânului din ambele specii.
Deoarece insulina umană recombinantă este identică cu hormonul endogen, nu s-au efectuat studii de reproducere / fertilitate la animale.
graviditate
Efecte teratogene
Sarcina Categorie C
Studiile de reproducere la animale nu au fost efectuate cu Exubera. De asemenea, nu se știe dacă Exubera poate provoca leziuni fetale atunci când este administrată unei femei însărcinate sau dacă Exubera poate afecta capacitatea de reproducere. Exubera trebuie administrată unei femei însărcinate numai dacă este necesar în mod clar.
Mamele care alăptează
Multe medicamente, inclusiv insulina umană, sunt excretate în laptele uman. Din acest motiv, trebuie să aveți precauție atunci când Exubera este administrată unei femei care alăptează. Pacienții cu diabet care alăptează pot necesita ajustări în doza Exubera, planul de masă sau ambele.
Utilizare pediatrică
Nu au fost stabilite siguranța și eficacitatea pe termen lung a Exubera la pacienții pediatri (vezi FARMACOLOGIE CLINICĂ, Populații speciale).
Utilizare geriatrică
În studiile clinice de fază 2/3 controlată (n = 1975), Exubera a fost administrat la 266 de pacienți - 65 de ani și 30 de pacienți - 75 de ani. Majoritatea acestor pacienți au avut diabet de tip 2. Schimbarea în HbA1C și rata hipoglicemiei nu a diferit în funcție de vârstă.
top
Reactii adverse
Siguranța Exubera singur sau în combinație cu insulină subcutanată sau agenți orali a fost evaluat la aproximativ 2500 de pacienți adulți cu diabet de tip 1 sau de tip 2 care au fost expuși Exubera. Aproximativ 2000 de pacienți au fost expuși la Exubera mai mult de 6 luni și peste 800 de pacienți au fost expuși mai mult de 2 ani.
Evenimente adverse non-respiratorii
Evenimente adverse respiratorii raportate la ‰ ¥ 1% din 1977 la pacienții tratați cu exubera în studii clinice controlate în faza 2/3, indiferent de cauzalitate, includ (dar nu sunt limitate la următoarele):
Metabolice și nutriționale: hipoglicemie (vezi AVERTIZĂRI și PRECAUȚII)
Întregul corp: dureri în piept
Digestiv: gura uscată
Simțuri speciale: otită medie (diabetici pediatri de tip 1)
hipoglicemia
Ratele și incidența hipoglicemiei au fost comparabile între Exubera și insulina umană regulată subcutanată la pacienții cu diabet tip 1 și tip 2. La pacienții de tip 2 care nu au fost controlați în mod adecvat cu terapie cu un singur agent oral, adăugarea de Exubera a fost asociată cu o rată mai mare de hipoglicemie decât a fost adăugarea unui al doilea oral agent.
Dureri în piept
O serie de simptome diferite toracice au fost raportate ca reacții adverse și au fost grupate sub termenul nespecific dureri toracice. Aceste evenimente au avut loc la 4,7% dintre pacienții tratați cu Exubera și 3,2% dintre pacienții din grupurile comparative. Majoritatea (> 90%) dintre aceste evenimente au fost raportate ca fiind ușoare sau moderate. Doi pacienți din Exubera și unul din grupul comparator au întrerupt tratamentul din cauza durerilor toracice. Incidența evenimentelor adverse cu toate cauzalitățile legate de boala coronariană, cum ar fi angina pectorală sau infarctul miocardic a fost comparabilă în Exubera (0,7% angină pectorală; 0,7% infarct miocardic) și comparator (1,3% angină pectorală; 0.7% infarct miocardic) grupuri de tratament.
Gură uscată
Gura uscată a fost raportată la 2,4% dintre pacienții tratați cu Exubera și 0,8% dintre pacienții din grupele comparative. Aproape toate (> 98%) din gura uscată raportată au fost ușoare sau moderate. Niciun pacient nu a întrerupt tratamentul din cauza gurii uscate.
Evenimente la urechi în diabetici pediatri
Diabeticii pediatrici de tip 1 din grupele Exubera au prezentat evenimente adverse legate de ureche mai frecvent decât diabeticii de tip 1 pediatru din grupurile de tratament care primesc doar insulină subcutanată. Aceste evenimente au inclus otită medie (Exubera 6,5%; SC 3,4%), dureri de ureche (Exubera 3,9%; SC 1,4%) și tulburări ale urechii (Exubera 1,3%; SC 0%).
Evenimente adverse respiratorii
Tabelul 6 arată incidența evenimentelor adverse respiratorii pentru fiecare grup de tratament care a fost raportat în ‰ ¥ 1% din orice grup de tratament din faza 2 și 3 studii clinice controlate, indiferent de cauzalitate.
Tabelul 6: Evenimente adverse respiratorii raportate în ‰ ¥ 1% din orice grup de tratament în studiile clinice de faza 2 și 3 controlate, indiferent de cauzalitate
| Procentul pacienților care raportează evenimentul | |||||
|---|---|---|---|---|---|
| Eveniment advers | Diabetul de tip 1 | Diabetul de tip 2 | |||
| Exubera N = 698 |
SC N = 705 |
Exubera N = 1279 |
SC N = 488 |
OAS N = 644 |
|
| SC = comparator de insulină subcutanată; OA = comparatori de agenți orali | |||||
| Infecția tractului respirator | 43.3 | 42.0 | 29.2 | 38.1 | 19.7 |
| Tuse crescută | 29.5 | 8.8 | 21.9 | 10.2 | 3.7 |
| Faringită | 18.2 | 16.6 | 9.5 | 9.6 | 5.9 |
| rinita | 14.5 | 10.9 | 8.8 | 10.5 | 3.0 |
| sinuzita | 10.3 | 7.4 | 5.4 | 10.0 | 2.3 |
| Tulburări respiratorii | 7.4 | 4.1 | 6.1 | 10.2 | 1.7 |
| Dispneea | 4.4 | 0.9 | 3.6 | 2.5 | 1.4 |
| Sputa crescută | 3.9 | 1.3 | 2.8 | 1.0 | 0.5 |
| Bronşită | 3.2 | 4.1 | 5.4 | 3.9 | 4.0 |
| Astm | 1.3 | 1.3 | 2.0 | 2.3 | 0.5 |
| epistaxis | 1.3 | 0.4 | 1.2 | 0.4 | 0.8 |
| Laringită | 1.1 | 0.4 | 0.5 | 0.4 | 0.3 |
| Pneumonie | 0.9 | 1.1 | 0.9 | 1.6 | 0.6 |
| Alterarea vocii | 0.1 | 0.1 | 1.3 | 0.0 | 0.3 |
Tuse
În 3 studii clinice, pacienții care au completat un chestionar pentru tuse au raportat că tuseul a avut tendința să apară în interior secunde până la minute după inhalarea Exubera, a fost predominant ușoară în severitate și a fost rar productivă în interior natură. Incidența acestei tuse a scăzut odată cu utilizarea continuă a Exubera. În studiile clinice controlate, 1,2% dintre pacienți au întrerupt tratamentul cu Exubera din cauza tusei.
Dispneea
Aproape toate (> 97%) dispnee au fost raportate ca fiind ușoare sau moderate. Un număr mic de pacienți tratați cu Exubera (0,4%) au întrerupt tratamentul din cauza dispneei, comparativ cu 0,1% dintre pacienții tratați comparativ.
Alte evenimente adverse respiratorii - faringita, sputa crescută și epistaxisul
Majoritatea acestor evenimente au fost raportate ca fiind ușoare sau moderate. Un număr mic de pacienți tratati cu Exubera au întrerupt tratamentul din cauza faringitei (0,2%) și a sputei a crescut (0,1%); niciun pacient nu a întrerupt tratamentul din cauza epistaxisului.
Funcția pulmonară
Efectul Exubera asupra sistemului respirator a fost evaluat la peste 3800 de pacienți în studii clinice de fază 2 și 3 controlate (în care 1977 au fost tratați cu Exubera). În studiile clinice randomizate, cu etichetă deschisă, cu o durată de până la doi ani, au fost tratați pacienți tratați cu Exubera a demonstrat o scădere mai mare a funcției pulmonare, în special volumul expirator forțat într-un singur al doilea (FEV1) și capacitatea de difuzie a monoxidului de carbon (DL)CO), decât pacienții tratați comparativ. Diferențele medii ale grupului de tratament în FEV1 și DLCO, au fost observate în primele câteva săptămâni de tratament cu Exubera și nu au progresat în perioada de tratament de doi ani. Într-un studiu clinic controlat finalizat la pacienții cu diabet zaharat tip 2 după doi ani de tratament cu Exubera, pacienții au arătat rezoluția diferenței de grup de tratament în FEV1 la șase săptămâni după întreruperea terapiei. Rezolvarea efectului Exubera asupra funcției pulmonare la pacienții cu diabet zaharat tip 1 nu a fost studiată după un tratament de lungă durată.
Figurile 3 până la 6 afișează media FEV1 și DLCO schimbare de la nivelul inițial față de timp, de la două studii în curs de randomizare, open-label, de doi ani, la 580 de pacienți cu tip 1 și 620 pacienți cu diabet de tip 2.
Figura 3: Schimbare de la valoarea de bază FEV1 (L) la pacienții cu diabet zaharat de tip 1 (medie +/- abatere standard)
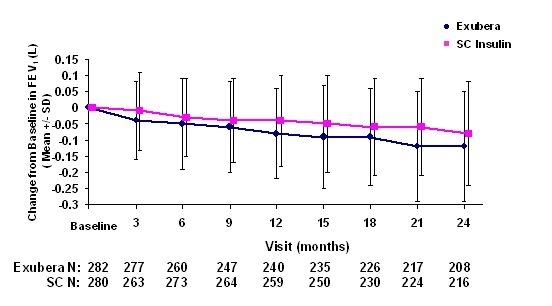
Figura 4: Schimbare de la valoarea de bază FEV1 (L) la pacienții cu diabet zaharat tip 2 (medie +/- abatere standard)
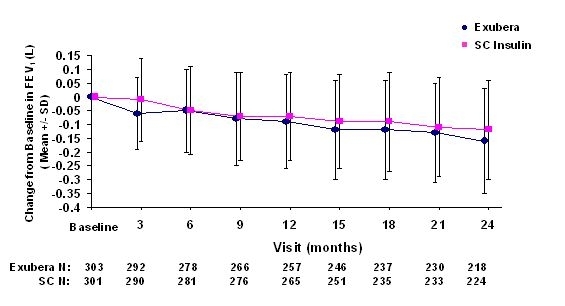
După 2 ani de tratament cu Exubera la pacienții cu diabet de tip 1 și tip 2, diferența între grupurile de tratament pentru modificarea medie de la valoarea inițială FEV1 a fost de aproximativ 40 ml, favorizând comparator.
Figura 5: Schimbare de la DLco de bază (mL / min / mmHg) la pacienții cu diabet zaharat tip 1 (medie +/- abatere standard)
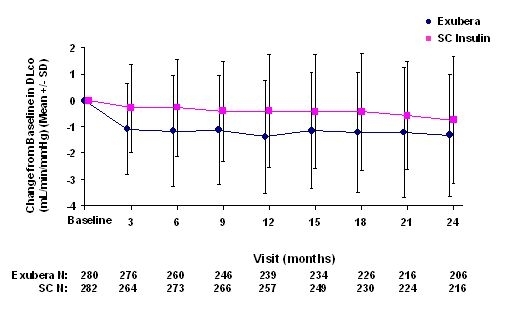
Figura 6: Schimbare de la DLco de bază (mL / min / mmHg) la pacienții cu diabet zaharat de tip 2 (medie +/- abatere standard)
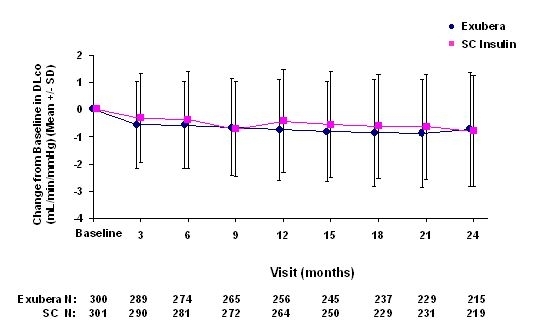
Dupa 2 ani de tratament cu Exubera, diferenta dintre grupurile de tratament pentru modificarea medie fata de DL de bazaCO a fost de aproximativ 0,5mL / min / mmHg (diabet tip 1), favorizând comparatorul și aproximativ 0,1 ml / min / mmHg (diabet tip 2), favorizând Exubera.
În timpul studiilor clinice de doi ani, pacienții individuali au înregistrat scăderi notabile ale funcției pulmonare în ambele grupuri de tratament. O scădere de la valoarea de bază FEV1 de la ‰ ¥ 20% la ultima observație au avut loc la 1,5% dintre pacienții tratați cu Exubera și 1,3% dintre pacienții tratați comparativ. O scădere din DL-ul de bazăCO 20% la ultima observație au avut loc la 5,1% dintre pacienții tratați cu Exubera și 3,6% dintre pacienții tratați comparativ.
top
Supradozarea
Hipoglicemia poate apărea ca urmare a unui exces de insulină în raport cu aportul alimentar, cheltuielile de energie sau ambele.
Episoadele ușoare până la moderate de hipoglicemie pot fi de obicei tratate cu glucoză orală. Poate fi necesară ajustarea dozelor de medicamente, a modelelor de masă sau a exercițiilor fizice.
Episoadele severe de hipoglicemie cu comă, convulsie sau afectare neurologică pot fi tratate cu glucagon intramuscular / subcutanat sau glucoză intravenoasă concentrată. Pot fi necesare aportul și observarea menținute de carbohidrați, deoarece hipoglicemia poate reapărea după recuperarea clinică aparentă.
top
Dozaj si administrare
Exubera, ca și analogii cu insulină cu acțiune rapidă, are un debut mai rapid al activității de scădere a glucozei în comparație cu insulina umană obișnuită injectată subcutanat. Exubera are o activitate de scădere a glucozei, comparabilă cu insulina umană obișnuită injectată subcutanat și mai lungă decât insulina cu acțiune rapidă. Dozele de exubera trebuie administrate imediat înainte de mese (cu cel mult 10 minute înainte de fiecare masă).
La pacienții cu diabet zaharat tip 1, Exubera trebuie utilizat în regimuri care includ o insulină cu acțiune mai lungă. Pentru pacienții cu diabet zaharat tip 2, Exubera poate fi utilizat ca monoterapie sau în combinație cu agenți orali sau insulină cu acțiune mai lungă.
Din cauza efectului Exubera asupra funcției pulmonare, toți pacienții ar trebui să aibă evaluată funcția pulmonară înainte de inițierea terapiei cu Exubera. Monitorizarea periodică a funcției pulmonare este recomandată pacienților tratați cu Exubera (vezi PRECAUȚII, Funcția pulmonară).
Exubera este destinat administrării prin inhalare și trebuie administrat numai cu Exubera® Inhalator. Consultați secțiunea Ghid pentru medicamente Exubera pentru o descriere a Exubera® Inhalator și instrucțiuni privind utilizarea inhalatorului.
Calculul dozei inițiale de pre-masă
Doza inițială de Exubera trebuie individualizată și determinată pe baza sfaturilor medicului, în conformitate cu nevoile pacientului. Dozele inițiale recomandate înainte de masă se bazează pe studiile clinice în care pacienților li s-a solicitat să mănânce trei mese pe zi. Dozele inițiale înainte de masă pot fi calculate folosind următoarea formulă: [Greutate corporală (kg) X 0,05 mg / kg = doza înainte de masă (mg)] rotunjită la cel mai apropiat număr de miligrame întreg (de exemplu, 3,7 mg rotunjit până la 3 mg).
Indicații aproximative pentru dozele inițiale, înainte de masă Exubera, pe baza greutății corporale a pacientului, sunt indicate în tabelul 7:
Tabelul 7: Orientări aproximative pentru doza de exubera inițială, înainte de masă (pe baza greutății corporale a pacientului)
| Greutatea pacientului (în kg) |
Greutatea pacientului (în lb) |
Doza inițială pe masă | Numărul de 1 mg Blistere pe doză | Număr blistere de 3 mg pe doză |
|---|---|---|---|---|
| 30 până la 39,9 kg | 66 - 87 lb | 1 mg pe masă | 1 | - |
| 40 până la 59,9 kg | 88 - 132 lb | 2 mg pe masă | 2 | - |
| 60 până la 79,9 kg | 133 - 176 lb | 3 mg pe masă | - | 1 |
| 80 până la 99,9 kg | 177 - 220 lb | 4 mg pe masă | 1 | 1 |
| 100 până la 119,9 kg | 221- 264 lb | 5 mg pe masă | 2 | 1 |
| 120 până la 139,9 kg | 265 - 308 lb | 6 mg pe masă | - | 2 |
Un blister de 1 mg de insulină inhalată Exubera este aproximativ echivalent cu 3 UI de insulină umană regulată injectată subcutanat. Un blister de 3 mg de insulină inhalată Exubera este aproximativ echivalent cu 8 UI de insulină umană regulată injectată subcutanat. Tabelul 8 oferă doza aproximativă de UI de insulină umană subcutanată obișnuită pentru doze de insulină inhalate Exubera de la 1 mg la 6 mg.
Tabelul 8: Doza UI echivalentă aproximativă a insulinei subcutanate umane obișnuite pentru doze de insulină inhalate Exubera cuprinse între 1 mg și 6 mg
| Doza (mg) | Doză aproximată de insulină SC regulată în UI | Numărul de 1 mg Blistere Exubera pe doză | Număr de bule Exubera de 3 mg pe doză |
|---|---|---|---|
| 1 mg | 3 | 1 | - |
| 2 mg | 6 | 2 | - |
| 3 mg | 8 | - | 1 |
| 4 mg | 11 | 1 | 1 |
| 5 mg | 14 | 2 | 1 |
| 6 mg | 16 | - | 2 |
Pacienții trebuie să combine 1 mg și 3 mg blistere, astfel încât să fie luat cel mai mic număr de blistere pe doză (de exemplu, o doză de 4 mg trebuie administrată ca un blister de 1 mg și un blister de 3 mg). Inhalarea consecutivă a trei blistere cu 1 unitate de doză determină o expunere la insulină semnificativ mai mare decât inhalarea unui blister de doză unitară de 3 mg. Prin urmare, trei doze de 1 mg nu trebuie înlocuite cu o doză de 3 mg (vezi FARMACOLOGIE CLINICĂ, Farmacocinetică). Când un pacient este stabilizat pe un regim de dozare care include blistere de 3 mg, și blistere de 3 mg devin temporar indisponibile, pacientul poate înlocui temporar două blistere de 1 mg cu 1 mg blister. Glicemia trebuie monitorizată îndeaproape.
La fel ca în cazul tuturor insulinelor, sunt incluși factori suplimentari care trebuie luați în considerare la determinarea dozei inițiale de Exubera nu se limitează la controlul glicemic actual al pacientului, răspunsul anterior la insulină, durata diabetului și alimentația și exercițiile fizice obiceiuri.
Considerații pentru titrarea dozei
După inițierea terapiei Exubera, ca și în cazul altor agenți de scădere a glucozei, poate fi necesară ajustarea dozei pe baza nevoia pacientului (de exemplu, concentrațiile de glucoză din sânge, mărimea mesei și compoziția de nutrienți, ora zilei și recent sau anticipat exercițiu). Fiecare pacient trebuie să fie titrat la doza optimă pe baza rezultatelor monitorizării glicemiei.
În ceea ce privește toate insulinele, cursul timpului acțiunii Exubera poate varia la diferiți indivizi sau în momente diferite la același individ.
Exubera poate fi utilizată în timpul bolilor respiratorii intercurente (de exemplu, bronșită, infecție a tractului respirator superior, rinită). Monitorizarea atentă a concentrațiilor de glucoză din sânge și ajustarea dozei poate fi necesară individual. Medicamentele inhalate (de exemplu, bronhodilatatoare) trebuie administrate înainte de administrarea de Exubera.
top
Cât este furnizat
Exubera (insulină umană [origine ADNc]) Inhalare Pulbere este disponibilă în blistere de 1 mg și 3 mg unitate de doză. Blisterele sunt distribuite pe carduri perforate de șase blistere cu doză unitară (PVC / aluminiu). Cele două puncte forte sunt diferențiate prin imprimare color și marcaje tactile care pot fi diferențiate prin atingere. Blisterele de 1 mg și cardurile perforate respective sunt imprimate cu cerneală verde, iar cardurile sunt marcate cu o bară ridicată. Blisterele de 3 mg și cardurile perforate respective sunt tipărite cu cerneală albastră, iar cardurile sunt marcate cu trei bare ridicate.
Cinci cărți de blister sunt ambalate într-o tavă termoformată din plastic (PET). Fiecare tavă PET conține, de asemenea, un desicant și este acoperită cu un capac de plastic transparent (PET). Tava de cinci carduri de blister (30 blistere cu doză unitară) este sigilată într-o pungă laminată cu folie cu un desicant.
Exubera (insulina umană [origine ADNc]) Inhalare Blistere pulbere, un Exubera® Inhalator și înlocuire Exubera® Unitățile de eliberare trebuie să inițieze terapia cu Exubera și sunt furnizate în kitul Exubera. Un Exubera complet asamblat® Inhalatorul este format din baza inhalatorului, o cameră și un Exubera® Unitatea de eliberare Un inhalator complet asamblat este ambalat cu o cameră de înlocuire și este disponibil în kitul Exubera și ca unitate separată. Camera este disponibilă și ca componentă individuală.
Exubera® Unitățile de eliberare sunt ambalate individual într-o tavă termoformată sigilată. Unul Exubera® Unitatea de eliberare este inclusă în fiecare inhalator complet asamblat. Două unități de eliberare suplimentare sunt furnizate în kitul Exubera și în fiecare pachet combinat. Unitățile de eliberare Exubera sunt de asemenea disponibile individual.
Vezi Tabelele 9 și 10 pentru o descriere a acestor configurații.
Tabelul 9
| Exubera (insulina umană [origine ADNc]) Pulbere de inhalare este disponibilă după cum urmează: | ||
|---|---|---|
| Descriere | Cuprins | NDC |
| KIT Exubera | 1 Inhalator Exubera 1 Camera de înlocuire 1 mg - 180 blistere 3 mg - 90 blistere 2 Exubera® Unități de eliberare |
0069-0050-85 |
| Pachet combinat Exubera 12 | 1 mg 90 blistere 3 mg - 90 blistere 2 Exubera® Unități de eliberare |
0069-0050-19 |
| Pachet combinat exubera 15 | 1 mg - 180 blistere 3 mg - 90 blistere 2 Exubera® Unități de eliberare |
0069-0050-53 |
| Pachet pacient exubera 1 mg | 90 ° 1 mg 2 Exubera® Unități de eliberare |
0069-0707-37 |
| Pachet pacient Exubera 3 mg | 90 ± 3 mg 2 Exubera® Unități de eliberare |
0069-0724-37 |
Tabelul 10
| Exubera® Inhalatorul și componentele sunt disponibile după cum urmează: | ||
|---|---|---|
| Descriere | Cuprins | NDC |
| Exubera® Inhalator & Camera | 1 Exubera® Inhalator 1 Camera de înlocuire |
0069-0054-19 |
| Exubera® Unități de eliberare | 2 Exubera® Unități de eliberare | 0069-0097-41 |
| Exubera® Cameră | 1 Camera de înlocuire | 0069-0061-19 |
Depozitare blister
Nu se folosește (nedeschis): Depozitați la temperatura camerei controlate, 25 ° C (77 ° F); excursii permise la 15-30 ° C (59-86 ° F) [a se vedea temperatura camerei controlate USP]. Nu înghețați. Nu refrigerați.
În utilizare: după deschiderea stratului de acoperire cu folie, blisterele cu doză unitară trebuie protejate de umiditate, depozitate la 25 ° C (77 ° F); excursii permise la 15-30 ° C (59-86 ° F) [a se vedea temperatura camerei controlate USP]. Nu înghețați. Nu refrigerați. Blisterele cu doză unitară trebuie utilizate în termen de 3 luni de la deschiderea supraîncărcării foliei. Întoarceți blisterele la înveliș pentru a vă proteja de umiditate. Trebuie să aveți grijă suplimentară pentru a evita mediile umede, de ex. baie aburită în urma unui duș.
Aruncați blisterul dacă este congelat.
Depozitare inhalator
A se păstra la temperatura camerei controlată, 25 ° C (77 ° F); excursii permise la 15-30 ° C (59-86 ° F) [a se vedea temperatura camerei controlate USP]. Nu înghețați. Nu refrigerați.
Exubera® Inhalatorul poate fi utilizat până la 1 an de la data primei utilizări.
Înlocuirea exuberei® Unitatea de eliberare
Exubera® Unitatea de eliberare din Exubera® Inhalatorul trebuie schimbat la fiecare 2 săptămâni.
A nu se lăsa la îndemâna copiilor
Numai Rx

LAB-0,331-12.0
ultima revizuire 04/2008
Exubera, insulină umană [origine ADNc] Informații despre pacient (în engleză simplă)
Informații detaliate despre semne, simptome, cauze, tratamente ale diabetului
Informațiile din această monografie nu sunt destinate să acopere toate utilizările posibile, indicații, precauții, interacțiuni medicamentoase sau efecte adverse. Aceste informații sunt generalizate și nu sunt destinate unor sfaturi medicale specifice. Dacă aveți întrebări despre medicamentele pe care le luați sau doriți mai multe informații, consultați medicul, farmacistul sau asistenta medicală.
înapoi la: Căutați toate medicamentele pentru diabet


