Janumet pentru tratamentul diabetului
Nume de marcă: Janumet
Denumire generică: Sitagliptin și Metformin Clorhidrat
Cuprins:
Indicații și utilizare
Dozaj si administrare
Forme de dozare și forțe
Contraindicații
Avertismente și precauții
Reactii adverse
Interacțiunile medicamentoase
Utilizare în populații specifice
Supradozaj
Descriere
Farmacologie
Toxicologie nonclinică
Studii clinice
Cât este furnizat
Informații despre consilierea pacientului
Janumet, Sitagliptin și Metformin Clorhidrat, Informații despre pacient (în engleză simplă)
AVERTIZARE: ACIDOZĂ LACTICĂ
Acidoza lactică este o complicație rară, dar gravă, care poate apărea din cauza acumulării de metformină. Riscul crește cu condiții precum sepsis, deshidratare, exces de alcool, insuficiență hepatică, insuficiență renală și insuficiență cardiacă congestivă acută.
Debutul este adesea subtil, însoțit doar de simptome nespecifice, cum ar fi stare de rău, mialgii, detresă respiratorie, somnolență și durere abdominală nespecifică. Anomaliile de laborator includ pH-ul scăzut, diferența crescută de anioni și lactatul crescut de sânge.
Dacă este suspectată acidoză, Janumet1 trebuie întreruptă și pacientul internat imediat. [Vedea Avertismente și precauții]
Indicații și utilizare
Janumet este indicat ca adjuvant la dieta și exerciții fizice pentru a îmbunătăți controlul glicemic la adulții cu diabet zaharat tip 2 când tratamentul cu sitagliptin și metformin este adecvat. [Vedea Studii clinice.]
Limitări importante de utilizare
Janumet nu trebuie utilizat la pacienții cu diabet zaharat tip 1 sau pentru tratamentul cetoacidozei diabetice, deoarece nu ar fi eficient în aceste setări.
Janumet nu a fost studiat în asociere cu insulina.
top
Dozaj si administrare
Dozare recomandată
Doza de terapie antihiperglicemică cu Janumet trebuie individualizată pe baza regimului actual al pacientului, eficacitatea și tolerabilitatea, fără a depăși doza maximă zilnică recomandată de 100 mg sitagliptin și 2000 mg metformină. Terapia combinată inițială sau întreținerea terapiei combinate trebuie individualizată și lăsată la latitudinea furnizorului de servicii medicale.
Janumet trebuie, în general, administrat de două ori pe zi, cu mese, cu escaladarea treptată a dozei, pentru a reduce efectele secundare gastrointestinale (GI) datorate metforminei.
Doza inițială de Janumet trebuie să se bazeze pe regimul curent al pacientului. Janumet trebuie administrat de două ori pe zi, împreună cu mesele. Sunt disponibile următoarele doze:
50 mg sitagliptin / 500 mg metformin clorhidrat
50 mg sitagliptin / 1000 mg clorhidrat de metformin.
Pacienții controlați inadecvat cu dieta și exercițiile fizice singuri
Dacă terapia cu o tabletă combinată care conține sitagliptin și metformină este considerată adecvată pentru un pacient cu diabet zaharat de tip 2 controlată necorespunzător numai cu dieta și exercițiile fizice, doza inițială recomandată este de 50 mg sitagliptin / 500 mg clorhidrat de metformină de două ori zilnic. Pacienții cu control glicemic inadecvat la această doză pot fi titrați până la 50 mg sitagliptin / 1000 mg clorhidrat de metformină de două ori pe zi.
Pacienții au controlat inadecvat monoterapia cu metformină
Dacă terapia cu un comprimat combinat care conține sitagliptin și metformin este considerată adecvată pentru un pacient controlat inadecvat doar pe metformină, doza inițială recomandată de Janumet trebuie să furnizeze sitagliptin doză de 50 mg de două ori pe zi (doză zilnică totală de 100 mg) și doza de metformină fiind deja Luat. Pentru pacienții care iau metformin 850 mg de două ori pe zi, doza inițială recomandată de Janumet este de 50 mg sitagliptin / 1000 mg clorhidrat de metformină de două ori pe zi.
Pacienții controlați inadecvat la monoterapia sitagliptinei
Dacă terapia cu o tabletă combinată care conține sitagliptin și metformină este considerată adecvată pentru un pacient inadecvat controlat doar pe sitagliptin, doza inițială recomandată de Janumet este de 50 mg sitagliptin / 500 mg clorhidrat de metformină de două ori zilnic. Pacienții cu un control inadecvat asupra acestei doze pot fi titrați până la 50 mg sitagliptin / 1000 mg clorhidrat de metformină de două ori pe zi. Pacienții care iau sitagliptin monoterapie ajustată la doză pentru insuficiență renală nu trebuie să fie comutați la Janumet [vezi Contraindicații].
Pacienții care au trecut de la administrarea concomitentă de sitagliptin și metformină
Pentru pacienții care au pornit de la sitagliptin concomitent cu metformin, Janumet poate fi inițiat la doza de sitagliptin și metformin luate deja.
Pacienții necorespunzători controlați pe terapia dublă combinație cu oricare dintre următorii agenți antihiperglicemici: sitagliptin, metformin sau sulfonilurea
Dacă terapia cu o tabletă combinată care conține sitagliptin și metformină este considerată adecvată în acest sens la setare, doza inițială obișnuită de Janumet trebuie să furnizeze sitagliptin doză de 50 mg de două ori pe zi (100 mg în total doza zilnica). Pentru a determina doza inițială a componentei metforminei, trebuie avut în vedere nivelul de control glicemic al pacientului și doza curentă (dacă există) de metformină. Trebuie luată în considerare escaladarea treptată a dozei pentru a reduce efectele secundare gastrointestinale (GI) asociate cu metformină. Pacienții aflați în prezent sau care inițiază o sulfonilurea pot necesita doze mai mici de sulfonilurea pentru a reduce riscul de hipoglicemie [vezi Avertismente și precauții].
Nu au fost efectuate studii care să examineze în mod specific siguranța și eficacitatea Janumet la pacienții tratați anterior cu alți agenți antihiperglucemici orali și au trecut la Janumet. Orice schimbare în terapia diabetului de tip 2 trebuie efectuată cu grijă și monitorizare adecvată, deoarece pot apărea modificări ale controlului glicemic.
top
Forme de dozare și forțe
- Comprimatele de 50 mg / 500 mg sunt comprimate acoperite cu peliculă roz-deschis, în formă de capsulă, cu „575” în relief pe o parte.
- Comprimatele de 50 mg / 1000 mg sunt comprimate filmate, în formă de capsulă, roșii, cu „577” în relief pe o parte.
top
Contraindicații
Janumet (sitagliptin / metformin HCl) este contraindicat la pacienții cu:
- Boală renală sau disfuncție renală, de exemplu, așa cum este sugerat de nivelurile de creatinină serică ‰ ¥ 1,5 mg / dL [bărbați], â ¥ 1,4 mg / dL [femei] sau anormale clearance-ul creatininei care poate rezulta și din afecțiuni precum colapsul cardiovascular (șoc), infarctul miocardic acut și septicemia [vedea Avertismente și precauții].
- Acidoză metabolică acută sau cronică, incluzând cetoacidoza diabetică, cu sau fără comă.
- Istoric de reacție de hipersensibilitate gravă la Janumet sau sitagliptin (una dintre componentele Janumet), cum ar fi anafilaxia sau angioedemul. [Vedea Avertismente și precauții și Reactii adverse.]
Janumet trebuie întrerupt temporar la pacienții supuși studiilor radiologice care implică intravasculare administrarea de materiale de contrast iodate, deoarece utilizarea unor astfel de produse poate duce la alterarea acută a sistemului renal funcție [vezi Avertismente și precauții].
top
Avertismente și precauții
Acidoză lactică
Clorhidrat de metformin
Acidoza lactică este o complicație metabolică rară, dar gravă, care poate apărea din cauza acumulării de metformină în timpul tratamentului cu Janumet; când apare, acesta este fatal în aproximativ 50% din cazuri. Acidoza lactică poate apărea, de asemenea, în asociere cu o serie de afecțiuni fiziopatologice, inclusiv diabetul zaharat, și ori de câte ori există hipoperfuzie tisulară și hipoxemie semnificativă. Acidoza lactică este caracterizată de niveluri crescute de lactat din sânge (> 5 mmol / L), scăderea pH-ului sanguin, tulburări de electroliți cu un decalaj crescut de anion și un raport crescut de lactat / piruvat. Când metformina este implicată ca cauză a acidozei lactice, se găsesc în general niveluri plasmatice de metformină> 5 μg / ml.
Incidența raportată a acidozei lactice la pacienții care primesc clorhidrat de metformină este foarte mică (aproximativ 0,03 cazuri / 1000 ani-pacient, cu aproximativ 0,015 cazuri fatale / 1000 pacient-ani). În mai mult de 20.000 de ani de pacienți expunerea la metformină în studiile clinice, nu a fost raportată acidoză lactică. Cazurile raportate au apărut în principal la pacienții diabetici cu insuficiență renală semnificativă, incluzând atât cele renale intrinseci boală și hipoperfuzie renală, adesea în stabilirea unor probleme medicale / chirurgicale concomitente multiple și concomitente multiple medicamente. Pacienții cu insuficiență cardiacă congestivă care necesită un tratament farmacologic, în special cei cu instabilitate sau insuficiența cardiacă acută congestivă, care prezintă risc de hipoperfuzie și hipoxemie, prezintă un risc crescut de lactice acidoza. Riscul de acidoză lactică crește odată cu gradul de disfuncție renală și vârsta pacientului. Prin urmare, riscul de acidoză lactică poate fi redus semnificativ prin monitorizarea periodică a funcției renale la pacienții care iau metformină și prin utilizarea dozei minime eficiente de metformină. În special, tratamentul vârstnicilor trebuie să fie însoțit de o monitorizare atentă a funcției renale. Tratamentul cu metformin nu trebuie inițiat la pacienți cu vârsta de 80 de ani, cu excepția măsurării clearance-ului creatininei demonstrează că funcția renală nu este redusă, deoarece acești pacienți sunt mai susceptibili să dezvolte acidoză lactică. În plus, metformina trebuie reținută imediat în prezența oricărei afecțiuni asociate cu hipoxemie, deshidratare sau sepsis. Deoarece funcția hepatică afectată poate limita semnificativ capacitatea de a curăța lactatul, metformina trebuie evitată, în general, la pacienții cu dovezi clinice sau de laborator ale bolii hepatice. Pacienții trebuie avertizați împotriva consumului excesiv de alcool, acut sau cronic, atunci când iau metformină, deoarece alcoolul potențează efectele clorhidratului de metformină asupra metabolismului lactatului. În plus, metformina trebuie întreruptă temporar înainte de orice studiu de radiocontrast intravascular și pentru orice procedură chirurgicală [vezi Avertismente și precauții].
Debutul acidozei lactice este adesea subtil și însoțit doar de simptome nespecifice, cum ar fi starea de rău, mialgii, detresă respiratorie, somnolență și durere abdominală nespecifică. Pot fi asociate hipotermie, hipotensiune arterială și bradiriotmii rezistente cu acidoză mai marcată. Pacientul și medicul pacientului trebuie să fie conștienți de importanța posibilă a unor astfel de simptome, iar pacientul trebuie să fie instruit să notifice imediat medicul dacă apare [vezi Avertismente și precauții]. Metformina trebuie retrasă până la clarificarea situației. Electroliți serici, cetone, glucoză din sânge și, dacă este indicat, pot fi utile pH-ul sângelui, nivelul lactatului și chiar nivelul metforminei din sânge. Odată ce un pacient este stabilizat la orice doză de metformină, este puțin probabil ca simptomele gastrointestinale să fie frecvente în timpul inițierii terapiei. Apariția ulterioară a simptomelor gastro-intestinale s-ar putea datora acidozei lactice sau altei boli grave.
Nivelurile de lactat plasmatic venos în condiții de depășire a limitei superioare a normalului, dar sub 5 mmol / L la pacienții care iau metformină nu indică neapărat lactice imminente acidoză și poate fi explicabilă prin alte mecanisme, cum ar fi diabetul zaharat sau obezitatea slab controlate, activitatea fizică viguroasă sau probleme tehnice în tratarea eșantionului [vedea Avertismente și precauții].
Acidoza lactică trebuie suspectată la orice pacient diabetic cu acidoză metabolică lipsită de dovezi de cetoacidoză (ketonurie și ketonemie).
Acidoza lactică este o urgență medicală care trebuie tratată într-un cadru spitalicesc. La un pacient cu acidoză lactică care ia metformină, medicamentul trebuie întrerupt imediat și instituite prompt măsuri generale de susținere. Deoarece clorhidratul de metformin este dializabil (cu un clearance de până la 170 ml / min sub o hemodinamică bună condiții), se recomandă hemodializă promptă pentru a corecta acidoza și a elimina acumulatul metformină. Un astfel de management duce adesea la o inversare promptă a simptomelor și recuperare [vezi Contraindicații; Avertismente și precauții].
Funcția hepatică afectată
Deoarece funcția hepatică afectată a fost asociată cu unele cazuri de acidoză lactică, Janumet trebuie evitat, în general, la pacienții cu dovezi clinice sau de laborator ale bolii hepatice.
Evaluarea funcției renale
Metformin și sitagliptin sunt cunoscute a fi substanțial excretate de rinichi. Riscul de acumulare de metformină și acidoză lactică crește odată cu gradul de afectare a funcției renale. Astfel, pacienții cu niveluri de creatinină serică peste limita superioară a normalului pentru vârsta lor nu trebuie să primească Janumet. La vârstnici, Janumet trebuie să fie titrat cu atenție pentru a stabili doza minimă pentru un efect glicemic adecvat, deoarece îmbătrânirea poate fi asociată cu funcția renală redusă. [Vedea Avertismente și precauții și Utilizare în populații specifice.]
Înainte de inițierea terapiei cu Janumet și cel puțin anual după aceea, funcția renală trebuie evaluată și verificată normal. La pacienții la care este prevăzută dezvoltarea unei disfuncții renale, în special la pacienții vârstnici, renală funcția ar trebui evaluată mai frecvent și Janumet a fost întrerupt dacă există dovezi de insuficiență renală prezent.
Vitamina B12 niveluri
În studiile clinice controlate cu metformină cu o durată de 29 de săptămâni, scăderea nivelurilor subnormale ale Vitinei B serice anterioare12 niveluri, fără manifestări clinice, au fost observate la aproximativ 7% dintre pacienți. O astfel de scădere, posibil datorită interferenței cu B12 absorbția din B12-complexul factorului intrinsec este totuși foarte rar asociat cu anemie și pare a fi repede reversibil cu întreruperea metforminei sau a vitaminei B12 suplimentarea. Măsurarea parametrilor hematologici pe o bază anuală este recomandată la pacienții aflați pe Janumet și orice anomalii aparente trebuie investigate și gestionate în mod corespunzător. [Vedea Reactii adverse.]
Anumiți indivizi (cei cu vitamina B inadecvată12 sau aportul de calciu sau absorbția) par a fi predispuși la dezvoltarea vitaminei B subnormale12 niveluri. La acești pacienți, Vitamina B serică de rutină12 Măsurătorile la intervale de doi-trei ani pot fi utile.
Aportul de alcool
Se știe că alcoolul potențează efectul metforminei asupra metabolismului lactatului. Prin urmare, pacienții trebuie avertizați împotriva consumului excesiv de alcool, acut sau cronic, în timp ce primesc Janumet.
Proceduri chirurgicale
Utilizarea Janumet trebuie suspendată temporar pentru orice intervenție chirurgicală (cu excepția procedurilor minore care nu sunt asociate cu aportul restricționat de alimente și lichide) și nu trebuie repornită până la reluarea aportului oral al pacientului și funcția renală a fost evaluată ca normal.
Modificarea stării clinice a pacienților cu diabet zaharat de tip 2 controlat anterior
Un pacient cu diabet zaharat tip 2 controlat anterior pe Janumet care dezvoltă anomalii de laborator sau clinice boala (în special boala vagă și slab definită) ar trebui evaluată prompt pentru dovezi de cetoacidoză sau lactică acidoza. Evaluarea trebuie să includă electroliți și cetone serice, glucoză în sânge și, dacă este indicat, pH-ul sângelui, lactat, piruvat și metformină. Dacă apare acidoză de oricare dintre forme, Janumet trebuie oprit imediat și inițiate alte măsuri corective adecvate.
Utilizați cu medicamente cunoscute pentru a cauza hipoglicemie
sitagliptinul
Așa cum este tipic în cazul altor agenți antihiperglicemici folosiți în combinație cu o sulfonilurea, când sitagliptin a fost utilizat în combinație cu metformină și sulfonilurea, un medicament cunoscut ca cauzând hipoglicemie, incidența hipoglicemiei a fost crescută față de cea a placebo în combinație cu metformină și sulfonilurea [vezi Reactii adverse]. De aceea, pacienții care primesc și un secretagog de insulină (de exemplu, sulfonilurea, meglitinidă) pot necesita o doză mai mică de secretagog insulină pentru a reduce riscul de hipoglicemie [vezi Dozaj si administrare].
Clorhidrat de metformin
Hipoglicemia nu apare la pacienții care primesc metformin singur în circumstanțele obișnuite de utilizare, dar poate apărea atunci când aportul caloric este deficitar, atunci când exercițiul intens nu este compensat prin suplimentarea calorică sau în timpul utilizării concomitente cu alți agenți de scădere a glucozei (cum ar fi sulfoniluree și insulină) sau etanol. Pacienții vârstnici, debilitați sau subnutriți și cei cu insuficiență suprarenală sau hipofizară sau intoxicații cu alcool sunt în special susceptibili la efecte hipoglicemice. Hipoglicemia poate fi dificil de recunoscut la vârstnici și la persoanele care iau droguri care blochează adrenergice β.
Medicamente concomitente care afectează funcția renală sau dispozitia metforminei
Medicamente (medicamente) concomitente care pot afecta funcția renală sau pot avea ca rezultat modificări hemodinamice semnificative interferează cu dispoziția metforminei, cum ar fi medicamentele cationice care sunt eliminate prin secreția tubulară renală [vedea Interacțiunile medicamentoase], trebuie utilizat cu precauție.
Studii radiologice cu materiale de contrast iodate intravasculare
Studii de contrast intravasculare cu materiale iodate (de exemplu, urogramă intravenoasă, colangiografie intravenoasă, angiografie și tomografii computerizate (tomografie computerizată)) cu materiale de contrast intravasculare) poate duce la alterarea acută a funcției renale și a fost asociată cu acidoza lactică la pacienții care primesc metformină [vezi Contraindicații]. Prin urmare, la pacienții la care este planificat un astfel de studiu, Janumet trebuie întrerupt temporar la momentul sau înainte de procedură și reținută timp de 48 de ore ulterior procedurii și reinstituită numai după ce funcția renală a fost reevaluată și găsită ca fii normal.
Statele hipoxice
Colaps cardiovascular (șoc) din orice cauză, insuficiență cardiacă congestivă acută, infarct miocardic acut și alte afecțiuni caracterizate prin hipoxemie au fost asociate cu acidoza lactică și pot provoca, de asemenea, prerenal azotemie. Atunci când astfel de evenimente apar la pacienții tratați cu Janumet, medicamentul trebuie întrerupt imediat.
Pierderea controlului glucozei din sânge
Când un pacient stabilizat la orice regim diabetic este expus la stres, cum ar fi febră, traume, infecții sau intervenții chirurgicale, poate apărea o pierdere temporară a controlului glicemic. În astfel de momente, poate fi necesar să rețineți Janumet și să administrați temporar insulina. Janumet poate fi reinstituit după rezolvarea episodului acut.
Reactii de hipersensibilitate
Au existat rapoarte postmarketing despre reacții de hipersensibilitate grave la pacienții tratați cu sitagliptin, una dintre componentele Janumet. Aceste reacții includ anafilaxia, angioedema și afecțiuni exfoliante ale pielii, inclusiv sindromul Stevens-Johnson. Deoarece aceste reacții sunt raportate voluntar de la o populație de dimensiuni incerte, este în general nu este posibil să estimați în mod fiabil frecvența lor sau să stabiliți o relație de cauzalitate cu expunerea la medicamente. Debutul acestor reacții a avut loc în primele 3 luni de la inițierea tratamentului cu sitagliptin, unele raportări apărând după prima doză. Dacă este suspectată o reacție de hipersensibilitate, întrerupeți Janumet, evaluați alte cauze potențiale ale evenimentului și instituiți un tratament alternativ pentru diabet. [Vedea Reactii adverse.]
Rezultate macrovasculare
Nu au existat studii clinice care să stabilească dovezi concludente privind reducerea riscului macrovascular cu Janumet sau cu orice alt medicament anti-diabetic.
top
Reactii adverse
Experiențe de studii clinice
Deoarece studiile clinice sunt efectuate în condiții variate, ratele de reacție adversă observate în studiile clinice ale a medicamentul nu poate fi comparat în mod direct cu ratele din studiile clinice ale unui alt medicament și poate să nu reflecte ratele observate în practică.
Sitagliptin și Metformin Administrarea concomitentă la pacienții cu diabet zaharat tip 2 controlat în mod inadecvat la dietă și exerciții fizice
Tabelul 1 prezintă cele mai frecvente reacții adverse (â ¥ 5% din pacienți) raportate (indiferent de evaluarea cauzalității de către investigator) într-o perioadă de 24 de săptămâni studiu factorial controlat cu placebo, în care sitagliptin și metformin au fost administrate concomitent la pacienții cu diabet zaharat tip 2, controlat în mod inadecvat la dietă și exercițiu.
Tabelul 1: Sitagliptin și Metformin co-administrate la pacienții cu diabet zaharat de tip 2, controlat în mod inadecvat la dietă și exerciții fizice: reacții adverse Raportat (indiferent de evaluarea cauzalității de către investigator) la ‰ ¥ 5% dintre pacienții care primesc terapie combinată (și mai mare decât la pacienții care primesc Placebo) *
| Număr de pacienți (%) | ||||
placebo |
sitagliptinul 100 mg QD |
Metformin 500 mg / Metformin 1000 mg licitat†|
sitagliptinul 50 mg ofertă + Metformin 500 mg / Metformin 1000 mg licitat†|
|
| N = 176 | N = 179 | N = 364†| N = 372†| |
| ||||
| Diaree | 7 (4.0) | 5 (2.8) | 28 (7.7) | 28 (7.5) |
| Infectia tractului respirator superior | 9 (5.1) | 8 (4.5) | 19 (5.2) | 23 (6.2) |
| Durere de cap | 5 (2.8) | 2 (1.1) | 14 (3.8) | 22 (5.9) |
Terapia suplimentară Sitagliptin la pacienții cu diabet zaharat de tip 2 controlat inadecvat pe Metformin singur
Într-un studiu controlat cu 24 de săptămâni placebo controlat cu sitagliptin 100 mg administrate o dată pe zi, adăugate la un regim de metformină de două ori pe zi, nu au fost reacții adverse raportate indiferent de evaluarea de către investigator a cauzalității la 5% dintre pacienți și mai frecvent decât la pacienții administrați placebo. Întreruperea terapiei din cauza reacțiilor adverse clinice a fost similară cu grupul de tratament cu placebo (sitagliptin și metformin, 1,9%; placebo și metformină, 2,5%).
hipoglicemia
Reacțiile adverse ale hipoglicemiei s-au bazat pe toate rapoartele de hipoglicemie; nu a fost necesară o măsurare concomitentă a glicemiei. Incidența globală a reacțiilor adverse specificate în prealabil la hipoglicemie la pacienții cu diabet zaharat tip 2, controlat în mod inadecvat la dieta și exercițiul fizic a fost de 0,6% în pacienți au primit placebo, 0,6% la pacienții care au primit sitagliptin singuri, 0,8% la pacienții care au primit metformin singur și 1,6% la pacienți care au primit sitagliptin în asociere cu metformină. La pacienții cu diabet zaharat tip 2 controlat inadecvat doar pe metformină, incidența generală a adverselor reacțiile de hipoglicemie au fost de 1,3% la pacienții cu administrare suplimentară de sitagliptin și 2,1% la pacienții care au primit supliment placebo.
Reacții adverse gastrointestinale
Incidențele experiențelor adverse preselecționate la pacienții tratați cu sitagliptin și metformin au fost similare cu cele raportate doar pentru pacienții tratați cu metformină. Vezi Tabelul 2.
Tabelul 2: Reacții adverse gastrointestinale preselecționate (indiferent de evaluarea cauzalității de către investigator) raportate la pacienții cu diabet zaharat tip 2 care primesc sitagliptin și metformin.
| Număr de pacienți (%) | ||||||
| Studiul Sitagliptin și Metformin la pacienții controlați inadecvat la dietă și exerciții fizice |
Studiul suplimentului Sitagliptin la pacienții controlați necorespunzător pe Metformin singur | |||||
placebo |
sitagliptinul 100 mg QD |
Metformin 500 mg / Metformin 1000 mg licitat* |
sitagliptinul 50 mg ofertă + Metformin 500 mg / Metformin 1000 mg licitat* |
Placebo și Metformin â € 1500 1500 mg zilnic |
Sitagliptin 100 mg QD și Metformin â € 1500 1500 mg zilnic |
|
| N = 176 | N = 179 | N = 364 | N = 372 | N = 237 | N = 464 | |
| ||||||
| Diaree | 7 (4.0) | 5 (2.8) | 28 (7.7) | 28 (7.5) | 6 (2.5) | 11 (2.4) |
| Greaţă | 2 (1.1) | 2 (1.1) | 20 (5.5) | 18 (4.8) | 2 (0.8) | 6 (1.3) |
| Vărsături | 1 (0.6) | 0 (0.0) | 2 (0.5) | 8 (2.2) | 2 (0.8) | 5 (1.1) |
| Durere abdominală†| 4 (2.3) | 6 (3.4) | 14 (3.8) | 11 (3.0) | 9 (3.8) | 10 (2.2) |
Sitagliptin în asociere cu Metformin și Glimepiridă
Într-un studiu de 24 de săptămâni controlat cu placebo asupra sitagliptin 100 mg ca terapie suplimentară la pacienții cu diabet zaharat tip 2, controlat inadecvat pe metformină și glimepiridă (sitagliptin, N = 116; placebo, N = 113), reacțiile adverse raportate indiferent de evaluarea de către investigator a cauzalității la 5% dintre pacienți tratate cu sitagliptin și mai frecvent decât la pacienții tratați cu placebo au fost: hipoglicemie (sitagliptin, 16,4%; placebo, 0,9%) și dureri de cap (6,9%, 2,7%).
Nu au fost observate modificări semnificative clinic ale semnelor vitale sau ale ECG (inclusiv în intervalul QTc) cu combinația de sitagliptin și metformin.
Cea mai frecventă experiență adversă în monoterapia sitagliptin raportată indiferent de investigator evaluarea cauzalității la 5% dintre pacienți și mai frecvent decât la pacienții care au primit placebo a fost rinofaringita.
Cele mai frecvente reacții adverse (> 5%) stabilite datorită inițierii terapiei cu metformină sunt diareea, greața / vărsăturile, flatulența, disconfortul abdominal, indigestia, astenia și cefaleea.
Teste de laborator
sitagliptinul
Incidența reacțiilor adverse de laborator a fost similară la pacienții tratati cu sitagliptin și metformin (7,6%) comparativ cu pacienții tratati cu placebo și metformin (8,7%). În majoritatea studiilor, dar nu în toate, o creștere mică a numărului de globule albe (aproximativ 200 de celule / microL diferență în WBC față de placebo; valoarea medie de bază WBC aproximativ 6600 celule / microL) a fost observată datorită creșterii mici a neutrofilelor. Această modificare a parametrilor de laborator nu este considerată relevantă din punct de vedere clinic.
Clorhidrat de metformin
În studiile clinice controlate cu metformină cu o durată de 29 de săptămâni, scăderea nivelurilor subnormale ale Vitinei B serice anterioare12 niveluri, fără manifestări clinice, au fost observate la aproximativ 7% dintre pacienți. O astfel de scădere, posibil datorită interferenței cu B12 absorbția din B12-complexul factorului intrinsec este totuși foarte rar asociat cu anemie și pare a fi repede reversibil cu întreruperea metforminei sau a vitaminei B12 suplimentarea. [Vedea Avertismente și precauții.]
Experiență postmarketing
Următoarele reacții adverse suplimentare au fost identificate în timpul utilizării postaproba a Janumet sau sitagliptin, una dintre componentele Janumet. Deoarece aceste reacții sunt raportate voluntar de la o populație de dimensiuni incerte, este în general nu este posibil să estimați în mod fiabil frecvența lor sau să stabiliți o relație de cauzalitate cu expunerea la medicamente.
Reacțiile de hipersensibilitate includ anafilaxie, angioedem, erupții cutanate, urticarie, vasculită cutanată și afecțiuni exfoliante ale pielii, inclusiv sindromul Stevens-Johnson [vezi Avertismente și precauții]; infectia tractului respirator superior; creșteri ale enzimelor hepatice; pancreatită.
top
Interacțiunile medicamentoase
Medicamente cationice
Medicamente cationice (de exemplu, amiloridă, digoxină, morfină, procainamidă, chinidină, chinină, ranitidină, triamteren, trimetoprim sau vancomicină) care sunt eliminat prin secreție tubulară renală are, teoretic, potențialul interacțiunii cu metformin, concurând pentru transportul tubular renal comun sisteme. O astfel de interacțiune între metformin și cimetidină orală a fost observată la voluntarii sănătoși normali atât în metformin-cimetidină cu o singură doză cât și în doză multiplă studii de interacțiune medicamentoasă, cu o creștere de 60% a plasmei de metformină maximă și a concentrațiilor de sânge integral și o creștere de 40% a plasmei și a metforminei din sânge integral ASC. În studiul cu o singură doză nu a existat nicio schimbare în timpul de înjumătățire prin eliminare. Metformin nu a avut niciun efect asupra farmacocineticii cimetidinei. Deși aceste interacțiuni rămân teoretice (cu excepția cimetidinei), monitorizarea atentă a pacientului și ajustarea dozei de Janumet și / sau medicamentul care interferează este recomandat la pacienții care iau medicamente cationice excretate prin secreția tubulară renală proximală sistem.
Digoxină
A existat o ușoară creștere a zonei de sub curbă (ASC, 11%) și a concentrației medii de vârf (C)max, 18%) digoxină cu administrarea concomitentă de 100 mg sitagliptin timp de 10 zile. Aceste creșteri nu sunt considerate a fi semnificative din punct de vedere clinic. Digoxina, ca medicament cationic, are potențialul de a concura cu metformina pentru sistemele tubulare renale comune, afectând astfel concentrațiile serice ale digoxinei, metforminei sau ambelor. Pacienții care primesc digoxină trebuie monitorizați în mod corespunzător. Nu se recomandă ajustarea dozei de digoxină sau Janumet.
Glyburida
Într-un studiu de interacțiune cu o singură doză la pacienții cu diabet zaharat de tip 2, administrarea concomitentă de metformin și glicburidă nu a avut ca rezultat nici o modificare în farmacocinetica metforminei și nici în farmacodinamică. Scade în ASC și C în glicurburămax au fost observate, dar au fost extrem de variabile. Natura cu o singură doză a acestui studiu și lipsa corelației dintre nivelurile de sânge ale glicarburilor și efectele farmacodinamice fac semnificația clinică a acestei interacțiuni.
furosemid
Un studiu de interacțiune medicamentoasă cu doză unică, metformin-furosemid la subiecți sănătoși a demonstrat că parametrii farmacocinetici ai ambilor compuși au fost afectați de administrarea concomitentă. Furosemidul a crescut plasma metforminei și sângele Cmax cu 22% și ASC de sânge cu 15%, fără nicio modificare semnificativă a clearance-ului renal de metformină. Când se administrează cu metformină, Cmax și ASC de furosemidă au fost cu 31% și respectiv cu 12% mai mici decât atunci când au fost administrate singure și Timpul de înjumătățire plasmatică final a fost redus cu 32%, fără modificări semnificative ale furosemidului renal clearance-ul. Nu sunt disponibile informații despre interacțiunea metforminei și furosemidului atunci când sunt administrate în mod cronic.
nifedipina
Un studiu de interacțiune cu o singură doză, metformin-nifedipină la voluntari sănătoși normali a demonstrat că administrarea concomitentă de nifedipină a crescut metformina C plasmaticămax și ASC cu 20% și respectiv 9% și au crescut cantitatea excretată în urină. Tmax iar timpul de înjumătățire nu a fost afectat. Nifedipina pare să îmbunătățească absorbția metforminei. Metformin a avut efecte minime asupra nifedipinei.
Utilizarea metforminei cu alte medicamente
Anumite medicamente tind să producă hiperglicemie și pot duce la pierderea controlului glicemic. Aceste medicamente includ tiazidele și alte diuretice, corticosteroizi, fenotiazine, produse tiroidiene, estrogeni, contraceptive orale, fenitoină, acid nicotinic, simpatomimetice, medicamente care blochează canalul de calciu și izoniazida. Când astfel de medicamente sunt administrate unui pacient care primește Janumet, pacientul trebuie să fie atent observat pentru a menține un control glicemic adecvat.
La voluntarii sănătoși, farmacocinetica metforminei și propranololului și a metforminei și ibuprofenului nu au fost afectate atunci când au fost administrate concomitent în studiile de interacțiune cu o singură doză.
Metformina este legată în mod neglijabil de proteinele plasmatice și, prin urmare, este mai puțin probabilă să interacționeze cu medicamente cu legături ridicate de proteine, cum ar fi salicilați, sulfonamide, cloramfenicol și probenecid, în comparație cu sulfonilureele, care sunt legate în mare măsură de ser proteine.
top
Utilizare în populații specifice
graviditate
Sarcina Categoria B:
Janumet
Nu există studii adecvate și bine controlate la gravide cu Janumet sau componentele sale individuale; prin urmare, nu este cunoscută siguranța Janumet la femeile gravide. Janumet trebuie utilizat în timpul sarcinii numai dacă este necesar în mod clar.
Merck & Co., Inc. ține un registru pentru a monitoriza rezultatele sarcinii femeilor expuse la Janumet în timpul sarcinii. Furnizorii de servicii medicale sunt încurajați să raporteze orice expunere prenatală la Janumet, apelând Registrul Sarcinii la (800) 986-8999.
Nu au fost efectuate studii pe animale cu produsele combinate din Janumet pentru a evalua efectele asupra reproducerii. Următoarele date se bazează pe descoperirile efectuate individual cu sitagliptin sau metformin.
sitagliptinul
Studiile de reproducere au fost efectuate la șobolani și iepuri. Dozele de sitagliptin până la 125 mg / kg (de aproximativ 12 ori expunerea umană la doza maximă recomandată la om) nu au afectat fertilitatea și nu au afectat fătul. Cu toate acestea, nu există studii adecvate și bine controlate cu sitagliptin la femeile gravide.
Sitagliptin administrată la șobolani și iepuri gravide din ziua de gestație 6 până la 20 (organogeneză) nu a fost teratogenă la doze orale de până la 250 mg / kg (șobolani) și 125 mg / kg (iepuri), sau de aproximativ 30 și 20 de ori expunerea umană la doza maximă recomandată la om (MRHD) de 100 mg / zi pe baza ASC comparații. Doze mai mari au crescut incidența malformațiilor de coaste la urmași la 1000 mg / kg, sau de aproximativ 100 de ori expunerea umană la MRHD.
Sitagliptin administrat la șobolani de sex feminin din ziua de gestație 6 până în ziua de alăptare 21 a scăzut greutatea corporală la urmașii de sex masculin și feminin la 1000 mg / kg. Nu a fost observată toxicitate funcțională sau comportamentală la descendența șobolanilor.
Transferul placentar de sitagliptin administrat la șobolani gravide a fost de aproximativ 45% la 2 ore și 80% la 24 ore după administrare. Transferul placentar de sitagliptin administrat la iepurii gravide a fost de aproximativ 66% la 2 ore și 30% la 24 de ore.
Clorhidrat de metformin
Metformin nu a fost teratogen la șobolani și iepuri la doze de până la 600 mg / kg / zi. Aceasta reprezintă o expunere de aproximativ 2 și 6 ori mai mare decât doza zilnică maximă recomandată de om de 2.000 mg pe baza comparațiilor cu suprafața corpului pentru șobolani și, respectiv, iepuri. Determinarea concentrațiilor fetale a demonstrat o barieră placentară parțială la metformină.
Mamele care alăptează
Nu au fost efectuate studii asupra animalelor care alăptează cu componentele combinate ale Janumet. În studiile efectuate cu componentele individuale, atât sitagliptina cât și metformina sunt secretate în laptele șobolanilor care alăptează. Nu se știe dacă sitagliptina este excretată în laptele uman. Deoarece multe medicamente sunt excretate în laptele uman, trebuie luată prudență atunci când Janumet este administrat unei femei care alăptează.
Utilizare pediatrică
Siguranța și eficacitatea Janumet la pacienții pediatri sub 18 ani nu au fost stabilite.
Utilizare geriatrică
Janumet
Deoarece sitagliptina și metformina sunt substanțial excretate de rinichi și deoarece îmbătrânirea poate fi asociată cu funcția renală redusă, Janumet trebuie utilizat cu precauție pe măsură ce crește vârsta. Trebuie avut grijă în selectarea dozei și trebuie să se bazeze pe o monitorizare atentă și regulată a funcției renale. [Vedea Avertismente și precauții; Farmacologie clinică.]
sitagliptinul
Din numărul total de subiecți (N = 3884) din studiile clinice din faza II și III asupra sitagliptinului, 725 de pacienți aveau 65 de ani și peste, în timp ce 61 de pacienți aveau peste 75 de ani. Nu au fost observate diferențe generale de siguranță sau eficacitate între subiecții de 65 de ani și peste și subiecții mai tineri. În timp ce aceasta și alte experiențe clinice raportate nu au identificat diferențe de răspuns între vârstnici și pacienți mai tineri nu poate fi o sensibilitate mai mare a unor persoane în vârstă exclus.
Clorhidrat de metformin
Studiile clinice controlate ale metforminei nu au inclus un număr suficient de pacienți vârstnici pentru a determina dacă aceștia răspund diferit de la pacienți mai tineri, deși alte experiențe clinice raportate nu au identificat diferențe de răspuns între vârstnici și tineri pacienți. Metformin trebuie utilizat doar la pacienții cu funcție renală normală. Dozarea inițială și de întreținere a metforminei trebuie să fie conservatoare la pacienții cu vârsta înaintată, datorită potențialului de scădere a funcției renale la această populație. Orice ajustare a dozei trebuie să se bazeze pe o evaluare atentă a funcției renale. [Vedea Contraindicații; Avertismente și precauții; și Farmacologie clinică.]
top
Supradozaj
sitagliptinul
În timpul studiilor clinice controlate la subiecți sănătoși, s-au administrat doze unice de până la 800 mg sitagliptin. Creșterea medie maximă a QTc de 8,0 msec a fost observată într-un studiu la o doză de 800 mg sitagliptin, un efect mediu care nu este considerat clinic important [vezi Farmacologie clinică]. Nu există experiență cu doze peste 800 mg la om. În studiile de doză multiplă în faza I, nu au fost observate reacții adverse clinice legate de doză cu sitagliptin, cu doze de până la 400 mg pe zi, pentru perioade de până la 28 de zile.
În caz de supradozaj, este rezonabil să folosiți măsurile de sprijin obișnuite, de exemplu, să eliminați materialul neabsorbit din gastrointestinal tratează, folosește monitorizare clinică (inclusiv obținerea unei electrocardiograme) și instituie terapie de susținere, după cum este indicat de pacientul clinic stare.
Sitagliptina este modest dializabilă. În studiile clinice, aproximativ 13,5% din doză a fost eliminată pe parcursul unei ședințe de hemodializă de 3 până la 4 ore. Hemodializa prelungită poate fi considerată dacă este adecvat din punct de vedere clinic. Nu se cunoaște dacă sitagliptina este dializabilă prin dializă peritoneală.
Clorhidrat de metformin
S-a produs supradozaj de clorhidrat de metformină, inclusiv ingestia unor cantități mai mari de 50 de grame. Hipoglicemia a fost raportată în aproximativ 10% din cazuri, dar nu s-a stabilit nicio asociere cauzală cu clorhidratul de metformină. Acidoza lactică a fost raportată la aproximativ 32% din cazurile de supradozaj cu metformină [vezi Avertismente și precauții]. Metformina este dializabilă cu un clearance de până la 170 ml / min în condiții bune hemodinamice. Prin urmare, hemodializa poate fi utilă pentru îndepărtarea medicamentului acumulat de la pacienții la care este suspectată supradozajul cu metformină.
top
Descriere
Janumet (sitagliptin / metformin HCl) comprimatele conțin două medicamente antihiperglucemice orale utilizate în tratamentul diabetului de tip 2: sitagliptin și clorhidrat de metformină.
sitagliptinul
Sitagliptin este un inhibitor activ oral al enzimei dipeptidil peptidaza-4 (DPP-4). Sitagliptin este prezent în comprimatele Janumet sub formă de fosfat de sitagliptin monohidrat. Sitagliptin fosfat monohidrat este descris chimic ca 7 - [(3R) - 3 - amino - 1 - oxo - 4 - (2,4,5 - trifluorfenil) butil] - 5,6,7,8 - tetrahidro - 3 - (trifluormetil) - 1,2,4 - triazolo [4,3 - a] pirazin fosfat (1: 1) monohidrat cu o formulă empirică din C16H15F6N5OH3PO4-H2O și o greutate moleculară de 523,32. Formula structurală este:
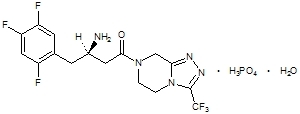
Sitagliptina fosfat monohidrat este o pulbere albă până la albă, cristalină, non-igroscopică. Este solubil în apă și N, N-dimetil formamidă; ușor solubil în metanol; foarte ușor solubil în etanol, acetonă și acetonitril; și insolubil în izopropanol și acetat de izopropil.
Clorhidrat de metformin
Clorhidratul de metformină (clorhidrat de N, N-dimetilimidodicarbonimidic) nu este legat chimic sau farmacologic de nici o altă clasă de agenți antihiperglicemici orali. Clorhidratul de metformină este un compus cristalin alb până la alb, cu o formulă moleculară de C4H11N5-HCl și o greutate moleculară de 165,63. Clorhidratul de metformin este solubil liber în apă și este practic insolubil în acetonă, eter și cloroform. PKA a metforminei este 12.4. PH-ul unei soluții apoase 1% de clorhidrat de metformină este 6,68. Formula structurală este după cum se arată:
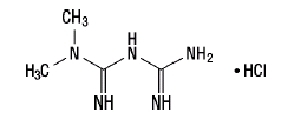
Janumet
Janumet este disponibil pentru administrare orală sub formă de tablete care conțin 64,25 mg sitagliptin fosfat monohidrat și echivalent clorhidrat de metformină până la: 50 mg sitagliptin sub formă de bază liberă și clorhidrat de metformin 500 mg (Janumet 50 mg / 500 mg) sau clorhidrat de metformină de 1000 mg (Janumet 50 mg / 1000 mg). Fiecare comprimat filmat de Janumet conține următoarele ingrediente inactive: celuloză microcristalină, polivinilpirolidonă, lauril sulfat de sodiu și fumarat de stearil de sodiu. În plus, acoperirea cu film conține următoarele ingrediente inactive: alcool polivinilic, polietilenglicol, talc, dioxid de titan, oxid roșu de fier și oxid de fier negru.
top
Farmacologie clinică
Mecanism de acțiune
Janumet
Janumet combină doi agenți antihiperglicemici cu mecanisme complementare de acțiune pentru îmbunătățirea controlului glicemic la pacienții cu diabet de tip 2: sitagliptin, un inhibitor al dipeptidil-peptidazei-4 (DPP-4) și clorhidrat de metformin, un membru al biguanidei clasă.
sitagliptinul
Sitagliptin este un inhibitor al DPP-4, despre care se crede că își exercită acțiunile la pacienții cu diabet de tip 2, încetinind inactivarea hormonilor incretinei. Concentrațiile hormonilor activi intacti sunt crescute de sitagliptin, crescând și prelungind acțiunea acestor hormoni. Hormoni cu incretină, incluzând peptida-1 asemănătoare glucagonului (GLP-1) și insulinotropă dependentă de glucoză polipeptida (GIP), sunt eliberate de intestin pe tot parcursul zilei, iar nivelurile sunt crescute ca răspuns la o masă. Acesti hormoni sunt inactivati rapid de enzima DPP-4. Incretinele fac parte dintr-un sistem endogen implicat în reglarea fiziologică a homeostazei cu glucoză. Atunci când concentrațiile de glucoză din sânge sunt normale sau crescute, GLP-1 și GIP cresc sinteza insulinei și eliberează din celulele beta pancreatice prin căi de semnalizare intracelulare care implică AMP ciclic. GLP-1 scade, de asemenea, secreția de glucagon din celulele alfa pancreatice, ceea ce duce la reducerea producției de glucoză hepatică. Prin creșterea și prelungirea nivelurilor de incretină activă, sitagliptina crește eliberarea de insulină și scade nivelul glucagonului în circulație într-un mod dependent de glucoză. Sitagliptin demonstrează selectivitate pentru DPP-4 și nu inhibă activitatea DPP-8 sau DPP-9 in vitro la concentrații apropiate de cele din doze terapeutice.
Clorhidrat de metformin
Metformin este un agent antihiperglicemic care îmbunătățește toleranța la glucoză la pacienții cu diabet zaharat tip 2, scăzând atât glucoza plasmatică bazală cât și cea postprandială. Mecanismele sale de acțiune farmacologice sunt diferite de alte clase de agenți antihiperglicemici orali. Metformin scade producția de glucoză hepatică, scade absorbția intestinală a glucozei și îmbunătățește sensibilitatea la insulină prin creșterea absorbției periferice a glicemiei și utilizarea. Spre deosebire de sulfoniluree, metformina nu produce hipoglicemie nici la pacienții cu diabet zaharat tip 2 sau la subiecți normali (cu excepția circumstanțelor speciale [vezi Avertismente și precauții]) și nu provoacă hiperinsulinemie. Odată cu terapia cu metformină, secreția de insulină rămâne neschimbată, în timp ce nivelul de insulină al jeunului și răspunsul insulinei plasmatice pe parcursul zilei pot scădea efectiv.
12.2 Farmacodinamica
sitagliptinul
General
La pacienții cu diabet zaharat de tip 2, administrarea sitagliptinei a dus la inhibarea activității enzimei DPP-4 pentru o perioadă de 24 de ore. După o încărcătură orală de glucoză sau o masă, această inhibare a DPP-4 a dus la o creștere de 2- 3 ori a nivelurilor circulante ale GLP-1 activ și GIP, scăderea concentrațiilor de glucagon și o reacție crescută la eliberarea insulinei la glucoză, ceea ce duce la creșterea peptidei C și a insulinei Concentrațiile. Creșterea insulinei cu scăderea glucagonului a fost asociată cu concentrații mai scăzute de glucoză pe post și reducerea excursiei de glucoză în urma unei încărcături orale de glucoză sau a unei mese.
Sitagliptin și Metformin clorhidrat Co-administrare
Într-un studiu de două zile la subiecți sănătoși, sitagliptin singur a crescut concentrațiile active de GLP-1, în timp ce metforminul singur a crescut concentrațiile active și totale de GLP-1 la valori similare. Administrarea concomitentă de sitagliptin și metformin a avut un efect aditiv asupra concentrațiilor active de GLP-1. Sitagliptin, dar nu și metformin, a crescut concentrațiile de GIP active. Nu este clar ce înseamnă aceste descoperiri pentru modificările controlului glicemic la pacienții cu diabet zaharat tip 2.
În studiile la subiecți sănătoși, sitagliptin nu a scăzut glicemia sau nu a provocat hipoglicemie.
Electrofiziologie cardiacă
Într-un studiu crossover randomizat, controlat cu placebo, la 79 de subiecți sănătoși li s-a administrat o singură doză orală de sitagliptin 100 mg, sitagliptin 800 mg (de 8 ori doza recomandată) și placebo. La doza recomandată de 100 mg, nu a existat niciun efect asupra intervalului QTc obținut la concentrația plasmatică maximă sau în orice alt moment în timpul studiului. În urma dozei de 800 mg, creșterea maximă a modificării medii corectate cu placebo în QTc de la valoarea inițială la 3 ore după administrare a fost de 8,0 msec. Această creștere nu este considerată semnificativă din punct de vedere clinic. La doza de 800 mg, concentrațiile plasmatice maxime ale plasagliptinei au fost de aproximativ 11 ori mai mari decât concentrațiile de vârf după o doză de 100 mg.
La pacienții cu diabet de tip 2 administrate sitagliptin 100 mg (N = 81) sau sitagliptin 200 mg (N = 63) zilnic, acolo nu au existat modificări semnificative în intervalul QTc pe baza datelor ECG obținute la momentul plasmei maxime așteptate concentraţie.
Farmacocinetica
Janumet
Rezultatele unui studiu de bioechivalență la subiecți sănătoși au demonstrat că Janumet (Hag sitagliptin / metformin) 50 mg / 500 comprimatele combinate mg și 50 mg / 1000 mg sunt bioechivalente la administrarea concomitentă a dozelor corespunzătoare de sitagliptin (JANUVIA™2) și clorhidrat de metformină sub formă de tablete individuale.
Absorbţie
sitagliptinul
Biodisponibilitatea absolută a sitagliptinei este de aproximativ 87%. Administrarea concomitentă a unei mese bogate în grăsimi cu sitagliptin nu a avut niciun efect asupra farmacocineticii sitagliptinei.
Clorhidrat de metformin
Biodisponibilitatea absolută a unei tablete de 500 mg clorhidrat de metformin administrată în condiții de post este de aproximativ 50-60%. Studiile care utilizează doze orale unice de comprimate clorhidrat de metformin 500 mg până la 1500 mg și 850 mg la 2550 mg, indică faptul că există lipsa proporționalității dozei cu doze crescânde, care se datorează scăderii absorbției, mai degrabă decât modificării eliminării Alimentele scad amploarea și întârzie ușor absorbția metforminei, așa cum se arată într-o concentrație plasmatică medie maximă cu aproximativ 40% mai mică (Cmax), o suprafață mai mică cu 25% sub concentrația plasmatică față de curba de timp (ASC) și o prelungire de 35 de minute a concentrației plasmatice maxime (Tmax) după administrarea unei singure comprimate de metformină de 850 mg cu alimente, comparativ cu aceeași tărie a tabletei administrată de post. Nu se cunoaște relevanța clinică a acestor scăderi.
distribuire
sitagliptinul
Volumul mediu de distribuție în stare constantă după o doză unică de 100 mg intravenos de sitagliptin la subiecții sănătoși este de aproximativ 198 litri. Fracția de sitagliptin legată reversibil de proteinele plasmatice este scăzută (38%).
Clorhidrat de metformin
Volumul aparent de distribuție (V / F) de metformină după doze orale unice de comprimate clorhidrat de metformin 850 mg a fost în medie de 654 ± 358 L. Metformina este legată în mod neglijabil de proteinele plasmatice, spre deosebire de sulfoniluree, care sunt mai mult de 90% legate de proteine. Metformin se desparte în eritrocite, cel mai probabil ca funcție a timpului. La doze clinice obișnuite și planificări de dozare a comprimatelor de clorhidrat de metformin, concentrațiile plasmatice de metformină în stare constantă sunt atinse în 24-48 de ore și sunt în general
Metabolism
sitagliptinul
Aproximativ 79% din sitagliptin este excretat neschimbat în urină, metabolismul fiind o cale minoră de eliminare.
În urma unui [14Doza orală de sitagliptin C, aproximativ 16% din radioactivitate a fost excretată ca metaboliți ai sitagliptin. Șase metaboliți au fost detectați la niveluri de urme și nu este de așteptat să contribuie la activitatea de inhibare plasmatică a DPP-4 a sitagliptinei. Studiile in vitro au indicat că enzima primară responsabilă pentru metabolismul limitat al sitagliptinei a fost CYP3A4, cu contribuția CYP2C8.
Clorhidrat de metformin
Studiile intravenoase cu o singură doză la subiecți normali demonstrează că metforminul este excretat neschimbat în urină și nu suferă metabolism hepatic (nu s-au identificat metaboliți la om) și nici biliar excreţie.
Excreţie
sitagliptinul
După administrarea unui oral [14Doza de sitagliptin la subiecți sănătoși, aproximativ 100% din radioactivitatea administrată a fost eliminată în materiile fecale (13%) sau în urină (87%) în decurs de o săptămână după administrare. Terminalul aparent t1/2 după o doză orală de sitagliptin de 100 mg a fost de aproximativ 12,4 ore, iar clearance-ul renal a fost de aproximativ 350 ml / min.
Eliminarea sitagliptinei are loc în principal prin excreția renală și implică secreție tubulară activă. Sitagliptin este un substrat pentru transportorul de anioni organici umani-3 (hOAT-3), care poate fi implicat în eliminarea renală a sitagliptinei. Nu a fost stabilită relevanța clinică a hOAT-3 în transportul sitagliptin. Sitagliptin este, de asemenea, un substrat al p-glicoproteinei, care poate fi implicat și în medierea eliminării renale a sitagliptinei. Cu toate acestea, ciclosporina, un inhibitor al p-glicoproteinei, nu a redus clearance-ul renal al sitagliptinei.
Clorhidrat de metformin
Clearance-ul renal este de aproximativ 3,5 ori mai mare decât clearance-ul creatininei, ceea ce indică faptul că secreția tubulară este calea principală de eliminare a metforminei. După administrarea orală, aproximativ 90% din medicamentul absorbit este eliminat pe cale renală în primele 24 de ore, cu un timp de înjumătățire plasmatică de eliminare de aproximativ 6,2 ore. În sânge, timpul de înjumătățire prin eliminare este de aproximativ 17,6 ore, ceea ce sugerează că masa eritrocitelor poate fi un compartiment de distribuție.
Populații speciale
Insuficiență renală
Janumet
Janumet nu trebuie utilizat la pacienții cu insuficiență renală [vezi Contraindicații; Avertismente și precauții].
sitagliptinul
A fost observată o creștere de aproximativ 2 ori a ASC plasmatic a sitagliptinei la pacienții cu insuficiență renală moderată și de aproximativ 4 ori a fost observată creștere la pacienții cu insuficiență renală severă, inclusiv la pacienții cu ESRD pe hemodializă, comparativ cu un control sănătos normal subiecți.
Clorhidrat de metformin
La pacienții cu funcție renală scăzută (bazată pe clearance-ul creatininei măsurate), timpul de înjumătățire plasmatică și sânge a metforminei este prelungită, iar clearance-ul renal este scăzut proporțional cu scăderea creatininei clearance-ul.
Insuficiență hepatică
sitagliptinul
La pacienții cu insuficiență hepatică moderată (scor Child-Pugh 7 la 9), înseamnă ASC și Cmax de sitagliptin a crescut cu aproximativ 21% și, respectiv, 13%, comparativ cu controalele potrivite sănătoase după administrarea unei singure doze de 100 mg de sitagliptin. Aceste diferențe nu sunt considerate semnificative din punct de vedere clinic.
Nu există experiență clinică la pacienții cu insuficiență hepatică severă (scorul Child-Pugh> 9).
Clorhidrat de metformin
Nu s-au efectuat studii farmacocinetice ale metforminei la pacienții cu insuficiență hepatică.
Sex
sitagliptinul
Sexul nu a avut niciun efect semnificativ din punct de vedere clinic asupra farmacocineticii sitagliptinei pe baza unui compozit analiza datelor farmacocinetice de faza I și a unei analize farmacocinetice a populației faza I și faza II date.
Clorhidrat de metformin
Parametrii farmacocinetici ai metforminei nu au diferit în mod semnificativ între subiecții normali și pacienții cu diabet zaharat tip 2 atunci când sunt analizați în funcție de gen. În mod similar, în studiile clinice controlate la pacienții cu diabet de tip 2, efectul antihiperglicemic al metforminei a fost comparabil la bărbați și femei.
geriatrie
sitagliptinul
Atunci când sunt luate în considerare efectele vârstei asupra funcției renale, numai vârsta nu a avut clinic impact semnificativ asupra farmacocineticii sitagliptinei pe baza unei farmacocinetice a populației analiză. Subiecții vârstnici (65 până la 80 de ani) au avut concentrații plasmatice de sitagliptin cu aproximativ 19% mai mari comparativ cu subiecții mai tineri.
Clorhidrat de metformin
Datele limitate din studiile farmacocinetice controlate asupra metforminei la subiecți vârstnici sănătoși sugerează că clearance-ul plasmatic total al metforminei este scăzut, timpul de înjumătățire plasmatică este prelungit și Cmax este crescută, comparativ cu subiecții tineri sănătoși. Din aceste date, se pare că modificarea farmacocineticii metforminei odată cu îmbătrânirea este contabilizată în principal de o modificare a funcției renale (vezi GLUCOPHAGE3 prescrierea informațiilor: FARMACOLOGIE CLINICĂ, Populații speciale, geriatrie).
Tratamentul cu Janumet nu trebuie inițiat la pacienți cu vârsta de 80 de ani, cu excepția cazului în care măsurarea clearance-ului creatininei demonstrează că funcția renală nu este redusă [vezi Avertismente și precauții].
de pediatrie
Nu au fost efectuate studii cu Janumet la pacienții pediatri.
Cursă
sitagliptinul
Rasa nu a avut niciun efect clinic semnificativ asupra farmacocineticii sitagliptinei pe baza unei analize compuse de date farmacocinetice disponibile, inclusiv subiecți de alb, hispanic, negru, asiatic și alte rasiale grupuri.
Clorhidrat de metformin
Nu s-au efectuat studii privind parametrii farmacocinetici ai metforminei în funcție de rasă. În studiile clinice controlate ale metforminei la pacienții cu diabet zaharat de tip 2, efectul antihiperglicemic a fost comparabil la alb (n = 249), negri (n = 51) și hispanici (n = 24).
Indicele masei corporale (IMC)
sitagliptinul
Indicele de masă corporală nu a avut niciun efect clinic semnificativ asupra farmacocineticii sitagliptinei pe baza unui compozit analiza datelor farmacocinetice de faza I și a unei analize farmacocinetice a populației faza I și faza II date.
Interacțiunile medicamentoase
Sitagliptin și clorhidrat de metformin
Administrarea concomitentă a mai multor doze de sitagliptin (50 mg) și metformină (1000 mg) administrate de două ori pe zi a făcut-o nu modifică în mod semnificativ farmacocinetica sitagliptinei sau metforminei la pacienții cu tipul 2 Diabet.
Nu au fost efectuate studii farmacocinetice de interacțiune cu Janumet; cu toate acestea, astfel de studii au fost efectuate cu componentele individuale ale Janumet (sitagliptin și clorhidrat de metformină).
sitagliptinul
Evaluarea in vitro a interacțiunilor medicamentoase
Sitagliptin nu este un inhibitor al izozimelor CYP CYP3A4, 2C8, 2C9, 2D6, 1A2, 2C19 sau 2B6 și nu este un inductor al CYP3A4. Sitagliptin este un substrat p-glicoproteină, dar nu inhibă transportul digoxinei mediat de p-glicoproteină. Pe baza acestor rezultate, sitagliptin este considerat puțin probabil să provoace interacțiuni cu alte medicamente care utilizează aceste căi.
Sitagliptina nu este legată în mare măsură de proteinele plasmatice. Prin urmare, înclinația sitagliptinei de a fi implicate în interacțiunile medicament-medicament semnificative din punct de vedere clinic mediate de deplasarea de legare a proteinelor plasmatice este foarte mică.
În evaluarea Vivo a interacțiunilor medicamentoase
Efectul Sitagliptin asupra altor medicamente
În studiile clinice, după cum s-a descris mai jos, sitagliptin nu a modificat în mod semnificativ farmacocinetica metforminei, glicburidei, simvastatinei, rosiglitazonei, warfarinei sau administrării orale contraceptive, care oferă dovezi in vivo a unei propensiuni scăzute pentru a provoca interacțiuni medicamentoase cu substraturile CYP3A4, CYP2C8, CYP2C9 și transportator cationic organic (OCT).
Digoxin: Sitagliptin a avut un efect minim asupra farmacocineticii digoxinei. După administrarea de 0,25 mg digoxină concomitent cu 100 mg sitagliptin zilnic timp de 10 zile, ASC plasmatic al digoxinei a fost crescut cu 11%, iar plasma Cmax cu 18%.
Sulfoniluree: farmacocinetica cu o singură doză a glicuridului, un substrat CYP2C9, nu a fost modificată în mod semnificativ la subiecții care au primit doze multiple de sitagliptină. Nu ar fi de așteptat interacțiuni semnificative din punct de vedere clinic cu alte sulfoniluree (de exemplu, glipizidă, tolbutamidă și glimepiridă) care, la fel ca glicurura, sunt eliminate în primul rând de CYP2C9 [vezi Avertismente și precauții].
Simvastatină: farmacocinetica cu o singură doză a simvastatinei, un substrat CYP3A4, nu a fost modificată în mod semnificativ la subiecții care au primit doze multiple zilnice de sitagliptină. Prin urmare, sitagliptin nu este un inhibitor al metabolismului mediat de CYP3A4.
Tiazolidinediones: farmacocinetica cu o singură doză a rosiglitazonei nu a fost modificată în mod semnificativ la subiecți primirea mai multor doze zilnice de sitagliptin, ceea ce indică faptul că sitagliptin nu este un inhibitor al CYP2C8 mediat metabolism.
Warfarină: Doze multiple zilnice de sitagliptin nu au modificat în mod semnificativ farmacocinetica, astfel cum a fost evaluată prin măsurarea Enantiomeri S (-) sau R (+) warfarină sau farmacodinamică (evaluată prin măsurarea protrombinei INR) a unei singure doze de warfarină. Deoarece S (-) warfarina este metabolizată în principal de CYP2C9, aceste date susțin și concluzia că sitagliptin nu este un inhibitor al CYP2C9.
Contraceptive orale: Administrarea concomitentă cu sitagliptin nu a modificat în mod semnificativ farmacocinetica în stare constantă a noretindronei sau a etinilestradiolului.
Efectul altor medicamente asupra Sitagliptin
Datele clinice descrise mai jos sugerează că sitagliptina nu este susceptibilă la interacțiuni semnificative din punct de vedere clinic prin administrarea concomitentă a medicamentelor.
Ciclosporină: Un studiu a fost realizat pentru a evalua efectul ciclosporinei, un puternic inhibitor al p-glicoproteinei, asupra farmacocineticii sitagliptinei. Administrarea concomitentă a unei singure doze orale de 100 mg de sitagliptin și a unei doze orale unice de 600 mg de ciclosporină au crescut ASC și Cmax de sitagliptin cu aproximativ 29%, respectiv 68%. Aceste modificări modeste în farmacocinetica sitagliptinei nu au fost considerate semnificative din punct de vedere clinic. Clearance-ul renal al sitagliptinei nu a fost modificat în mod semnificativ. Prin urmare, interacțiuni semnificative nu ar fi așteptate cu alți inhibitori de p-glicoproteină.
Clorhidrat de metformin
[Vedea Interacțiunile medicamentoase]
top
Toxicologie nonclinică
Carcinogeneza, mutageneza, afectarea fertilitatii
Janumet
Nu au fost efectuate studii la animale cu produsele combinate din Janumet pentru a evalua carcinogeneza, mutageneza sau deteriorarea fertilității. Următoarele date se bazează pe rezultatele obținute în studii cu sitagliptin și metformin individual.
sitagliptinul
Un studiu de doi ani asupra carcinogenității a fost efectuat la șobolani bărbați și femei, administrate în doze orale de sitagliptin de 50, 150 și 500 mg / kg / zi. A existat o incidență crescută a adenomului / carcinomului hepatic combinat la bărbați și femei și a carcinomului hepatic la femei la 500 mg / kg. Această doză are ca rezultat expuneri de aproximativ 60 de ori expunerea umană la doza maximă recomandată zilnic de adulți umani (MRHD) de 100 mg / zi pe baza comparațiilor ASC. Tumorile hepatice nu au fost observate la 150 mg / kg, de aproximativ 20 de ori expunerea umană la MRHD. Un studiu de doi ani asupra carcinogenității a fost efectuat la șoarecii de sex masculin și feminin, administrate în doze orale de sitagliptin de 50, 125, 250 și 500 mg / kg / zi. Nu a existat o creștere a incidenței tumorilor la niciun organ până la 500 mg / kg, de aproximativ 70 de ori expunerea umană la MRHD. Sitagliptin nu a fost mutagenă sau clastogenă cu sau fără activare metabolică în testul de mutagenicitate bacterian Ames, un ovar de hamster chinez (CHO) test de aberație cromozomială, test de citogenetică in vitro în CHO, analiză de eluție a ADN-ului hepatocit in vitro de șobolan și micronucleu in vivo test.
În studiile de fertilitate la șobolan, cu doze de gavaj oral de 125, 250 și 1000 mg / kg, bărbații au fost tratați timp de 4 săptămâni înainte de împerechere, în timpul împerecherea, până la terminarea programată (aproximativ 8 săptămâni în total), iar femelele au fost tratate cu 2 săptămâni înainte de împerechere prin gestație ziua 7 Nu s-a observat niciun efect advers asupra fertilității la 125 mg / kg (de aproximativ 12 ori expunerea umană la MRHD de 100 mg / zi pe baza comparațiilor ASC). La doze mai mari, au fost observate resorbții crescute legate de nondose la femei (aproximativ 25 și 100 de ori expunerea umană la MRHD pe baza comparației ASC).
Clorhidrat de metformin
Studii de carcinogenitate pe termen lung au fost efectuate la șobolani (durata de administrare a 104 săptămâni) și șoareci (durata de administrare a 91 săptămâni) în doze de până la 900 mg / kg / zi și 1500 mg / kg / zi, inclusiv respectiv. Aceste doze sunt de aproximativ patru ori mai mari decât doza zilnică maximă recomandată umană de 2000 mg pe baza comparațiilor cu suprafața corpului. Nu s-au găsit dovezi de carcinogenitate cu metformină la șoarecii de sex masculin sau feminin. În mod similar, la șobolanii de sex masculin nu s-a observat niciun potențial tumorigenic cu metformină. Cu toate acestea, a existat o incidență crescută de polipi uterini benigni stromali la șobolani de sex feminin tratate cu 900 mg / kg / zi.
Nu a existat nicio dovadă a unui potențial mutagen al metforminei în următoarele teste in vitro: Test Ames (S. tifimuriu), test de mutație a genelor (celule de limfom de șoarece) sau test de aberații cromozomiale (limfocite umane). Rezultatele testului in vivo al micronucleului la șoarece au fost, de asemenea, negative. Fertilitatea șobolanilor de sex masculin sau feminin nu a fost afectată de metformină atunci când a fost administrată în doze de până la 600 mg / kg / zi, care este de aproximativ trei ori mai mare decât doza zilnică maximă recomandată de om pe baza suprafeței corpului comparații.
top
Studii clinice
Administrarea concomitentă de sitagliptin și metformin a fost studiată la pacienții cu diabet zaharat de tip 2, controlat în mod inadecvat la dietă și exerciții fizice și în combinație cu glimepirida.
Nu au fost efectuate studii clinice privind eficacitatea efectuate cu Janumet; cu toate acestea, a fost demonstrată bioechivalența Janumet cu sitagliptin și comprimate clorhidrat de metformin.
Sitagliptin și Metformin Administrarea concomitentă la pacienții cu diabet zaharat tip 2 controlat în mod inadecvat la dietă și exerciții fizice
La un interval de 24 de săptămâni au participat un număr de 1091 de pacienți cu diabet zaharat tip 2 și un control glicemic inadecvat asupra dietei și exercițiilor fizice; studiu factorial randomizat, dublu orb, controlat cu placebo, conceput pentru a evalua eficacitatea sitagliptinei și a metforminei administrarea concomitentă. Pacienții cu un agent antihiperglicemic (N = 541) au suferit o dietă, exerciții fizice și o perioadă de spălare a medicamentelor cu o durată de până la 12 săptămâni. După perioada de spălare, pacienții cu un control glicemic necorespunzător (A1C 7,5% - 11%) au fost randomizați după finalizarea unei perioade de 2 săptămâni cu un placebo. Pacienți care nu au agenți antihiperglicemici la intrarea în studiu (N = 550) cu control glicemic inadecvat (A1C 7,5% până la 11%) au intrat imediat în perioada de 2 săptămâni cu un placebo pentru a intra în plasă și apoi au fost randomizat. Aproximativ un număr egal de pacienți au fost randomizați pentru a primi placebo, 100 mg sitagliptin o dată pe zi, 500 mg sau 1000 mg de metformină de două ori pe zi sau 50 mg de sitagliptin de două ori pe zi în combinație cu 500 mg sau 1000 mg de metformină de două ori zilnic. Pacienții care nu au reușit să îndeplinească obiective specifice glicemiei în timpul studiului au fost tratați cu salvare cu gliburidă (glibenclamidă).
Administrarea concomitentă de Sitagliptin și metformin a furnizat îmbunătățiri semnificative ale A1C, FPG și PPG de 2 ore în comparație cu placebo, doar cu metformină și sitagliptin singur (tabelul 3, figura 1). Reducerile medii de la valoarea inițială în A1C au fost, în general, mai mari pentru pacienții cu valori inițiale mai mari ale A1C. Pentru pacienții care nu se află într-un agent antihiperglicemic la intrarea în studiu, reducerile medii de la nivelul inițial în A1C au fost: sitagliptin 100 mg o dată pe zi, -1,1%; metformin 500 mg ofertă, -1,1%; metformin 1000 mg ofertă, -1,2%; sitagliptin ofertă de 50 mg cu metformin 500 mg licitație, -1,6%; sitagliptin ofertă de 50 mg cu metformin 1000 mg ofertă, -1,9%; și pentru pacienții care au primit placebo, -0,2%. Efectele lipidelor au fost în general neutre. Scăderea greutății corporale în grupurile administrate sitagliptin în asociere cu metformin a fost similară cu cea a grupurilor administrate cu metformină singură sau cu placebo.
Tabelul 3: Parametri glicemici la vizita finală (studiu de 24 de săptămâni) pentru Sitagliptin și Metformin, singur și în combinație la pacienții cu diabet zaharat tip 2, controlat în mod inadecvat la dietă și exercițiu *
placebo |
sitagliptinul 100 mg QD |
Metformina 500 mg ofertă |
Metformina 1000 mg ofertă |
sitagliptinul 50 mg ofertă + Metformina 500 mg ofertă |
sitagliptinul 50 mg ofertă + Metformina 1000 mg ofertă |
|
| ||||||
| A1C (%) | N = 165 | N = 175 | N = 178 | N = 177 | N = 183 | N = 178 |
| Linie de bază (medie) | 8.7 | 8.9 | 8.9 | 8.7 | 8.8 | 8.8 |
| Modificarea de la linia de bază (media ajustată†) | 0.2 | -0.7 | -0.8 | -1.1 | -1.4 | -1.9 |
| Diferența față de placebo (media ajustată†) (IC 95%) |
-0.8c (-1.1, -0.6) |
-1.0c (-1.2, -0.8) |
-1.3c (-1.5, -1.1) |
-1.6c (-1.8, -1.3) |
-2.1c (-2.3, -1.8) |
|
| Pacienți (%) care ating A1C <7% | 15 (9%) | 35 (20%) | 41 (23%) | 68 (38%) | 79 (43%) | 118 (66%) |
| % Pacienți care primesc medicamente de salvare | 32 | 21 | 17 | 12 | 8 | 2 |
| FPG (mg / dL) | N = 169 | N = 178 | N = 179 | N = 179 | N = 183 | N = 180 |
| Linie de bază (medie) | 196 | 201 | 205 | 197 | 204 | 197 |
| Modificarea de la linia de bază (media ajustată†) | 6 | -17 | -27 | -29 | -47 | -64 |
| Diferența față de placebo (media ajustată†) (IC 95%) |
-23c (-33, -14) |
-33c (-43, -24) |
-35c (-45, -26) |
-53c (-62, -43) |
-70c (-79, -60) |
|
| PPG de 2 ore (mg / dL) | N = 129 | N = 136 | N = 141 | N = 138 | N = 147 | N = 152 |
| Linie de bază (medie) | 277 | 285 | 293 | 283 | 292 | 287 |
| Modificarea de la linia de bază (media ajustată†) | 0 | -52 | -53 | -78 | -93 | -117 |
| Diferența față de placebo (media ajustată†) (IC 95%) |
-52c (-67, -37) |
-54c (-69, -39) |
-78c (-93, -63) |
-93c (-107, -78) |
-117c (-131, -102) |
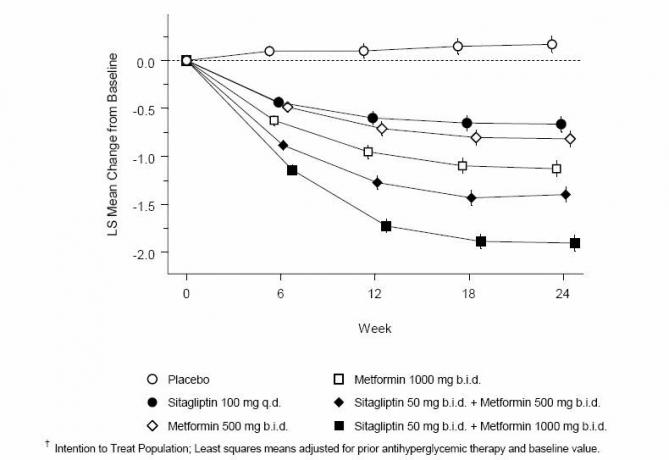
Figura 1: Modificarea medie de la valoarea inițială pentru A1C (%) pe 24 de săptămâni cu Sitagliptin și Metformin, singur și în asociere la pacienții cu diabet zaharat tip 2 controlat în mod inadecvat cu dieta și exercițiile fizice ”
În plus, acest studiu a inclus pacienți (N = 117) cu hiperglicemie mai severă (A1C> 11% sau sânge glucoză> 280 mg / dL) care au fost tratate cu sitagliptin de 50 de ori pe etichetă deschisă și metformin 1000 mg. La acest grup de pacienți, valoarea medie de referință A1C a fost de 11,2%, FPG-ul mediu a fost de 314 mg / dL, iar media de PPG de 2 ore a fost de 441 mg / dL. După 24 de săptămâni, au fost observate scăderi medii de la nivelul inițial de -2,9% pentru A1C, -127 mg / dL pentru FPG și -208 mg / dL pentru 2 ore PPG.
Terapia combinată inițială sau întreținerea terapiei combinate trebuie individualizate și sunt lăsate la latitudinea furnizorului de servicii medicale.
Terapia suplimentară Sitagliptin la pacienții cu diabet zaharat de tip 2 controlat inadecvat pe Metformin singur
Un număr de 701 de pacienți cu diabet de tip 2 au participat la un studiu de 24 de săptămâni, randomizat, dublu-orb, controlat cu placebo, conceput pentru a evalua eficacitatea sitagliptinei în asociere cu metformin. Pacienții aflați deja în metformină (N = 431) la o doză de cel puțin 1500 mg pe zi au fost randomizați după ce au terminat o perioadă de 2 săptămâni, un singur placebo, cu un placebo. Pacienți cu metformină și un alt agent antihiperglicemic (N = 229) și pacienți care nu au niciun agent antihiperglicemic (în afara terapiei pentru cel puțin 8 săptămâni, N = 41) au fost randomizate după o perioadă de rodaj de aproximativ 10 săptămâni pe metformină (la o doză de cel puțin 1500 mg pe zi) în în monoterapie. Pacienții au fost randomizați la adăugarea a 100 mg de sitagliptin sau placebo, administrate o dată pe zi. Pacienții care nu au reușit să îndeplinească obiective specifice glicemiei în timpul studiilor au fost tratați cu salvare cu pioglitazonă.
În combinație cu metformin, sitagliptin a furnizat îmbunătățiri semnificative ale A1C, FPG și PPG de 2 ore în comparație cu placebo cu metformin (tabelul 4). Terapia glicemică de salvare a fost utilizată la 5% dintre pacienții tratați cu sitagliptin 100 mg și 14% dintre pacienții tratați cu placebo. O scădere similară a greutății corporale a fost observată pentru ambele grupuri de tratament.
Tabelul 4: Parametri glicemici la vizita finală (studiu de 24 de săptămâni) al sitagliptinei în terapia combinată suplimentară cu metformină *
| Sitagliptin 100 mg QD + Metformin |
placebo + Metformin |
|
| ||
| A1C (%) | N = 453 | N = 224 |
| Linie de bază (medie) | 8.0 | 8.0 |
| Modificarea de la linia de bază (media ajustată†) | -0.7 | -0.0 |
| Diferența față de placebo + metformină (media ajustată†) (IC 95%) |
-0.7c (-0.8, -0.5) |
|
| Pacienți (%) care ating A1C <7% | 213 (47%) | 41 (18%) |
| FPG (mg / dL) | N = 454 | N = 226 |
| Linie de bază (medie) | 170 | 174 |
| Modificarea de la linia de bază (media ajustată†) | -17 | 9 |
| Diferența față de placebo + metformină (media ajustată†) (IC 95%) |
-25c (-31, -20) |
|
| PPG de 2 ore (mg / dL) | N = 387 | N = 182 |
| Linie de bază (medie) | 275 | 272 |
| Modificarea de la linia de bază (media ajustată†) | -62 | -11 |
| Diferența față de placebo + metformină (media ajustată†) (IC 95%) |
-51c (-61, -41) |
Terapia suplimentară Sitagliptin la pacienții cu diabet zaharat de tip 2 controlat în mod inadecvat în combinația de metformină și glimepiridă
Un total de 441 de pacienți cu diabet de tip 2 au participat la 24 de săptămâni, randomizate, dublu-orb, studiu controlat cu placebo conceput pentru a evalua eficacitatea sitagliptin în asociere cu glimepirida, cu sau fără metformină. Pacienții au intrat într-o perioadă de tratament cu glimepiridă (‰ ¥ 4 mg pe zi) singuri sau glimepiridă în combinație cu metformină (â ¥ 1500 mg pe zi). După o perioadă de titrare a dozei și intervalul de administrare stabil la doză de până la 16 săptămâni și o perioadă de 2 săptămâni de administrare placebo, pacienții cu insuficiență controlul glicemic (A1C de la 7,5% la 10,5%) au fost randomizate până la adăugarea a 100 mg sitagliptin sau placebo, administrate o dată zilnic. Pacienții care nu au reușit să îndeplinească obiective specifice glicemiei în timpul studiilor au fost tratați cu salvare cu pioglitazonă.
Pacienții care au primit sitagliptin cu metformin și glimepiridă au avut îmbunătățiri semnificative ale A1C și FPG, comparativ cu pacienții care au primit placebo cu metformină și glimepiridă (tabelul 5), cu reduceri medii de la valoarea inițială față de placebo în A1C de -0,9% și în FPG de -21 mg / dl. Terapia de salvare a fost utilizată la 8% dintre pacienții tratați cu sitagliptin 100 mg și 29% dintre pacienții tratați cu supliment placebo. Pacienții tratați cu sitagliptin suplimentar au avut o creștere medie a greutății corporale cu 1,1 kg vs. placebo suplimentar (+0,4 kg vs. -0,7 kg). În plus, sitagliptin suplimentar a dus la o rată crescută de hipoglucemie în comparație cu suplimentul placebo. [Vedea Avertismente și precauții; Reactii adverse.]
Tabelul 5: Parametri glicemici la vizita finală (studiu de 24 de săptămâni) pentru Sitagliptin în asociere cu Metformin și Glimepiride *
| Sitagliptin 100 mg + Metformin și Glimepirida |
placebo + Metformin și Glimepirida |
|
| ||
| A1C (%) | N = 115 | N = 105 |
| Linie de bază (medie) | 8.3 | 8.3 |
| Modificarea de la linia de bază (media ajustată†) | -0.6 | 0.3 |
| Diferența față de placebo (media ajustată†) (IC 95%) | -0.9c (-1.1, -0.7) |
|
| Pacienți (%) care ating A1C <7% | 26 (23%) | 1 (1%) |
| FPG (mg / dL) | N = 115 | N = 109 |
| Linie de bază (medie) | 179 | 179 |
| Modificarea de la linia de bază (media ajustată†) | -8 | 13 |
| Diferența față de placebo (media ajustată†) (IC 95%) | -21c (-32, -10) |
Terapia suplimentară Sitagliptin vs. Terapia suplimentară cu glipizidă la pacienții cu diabet zaharat de tip 2, controlată inadecvat pe metformină
Eficacitatea sitagliptin a fost evaluată într-un studiu de 52 de săptămâni, dublu orb, controlat de noninferioritate controlat de glipizide la pacienții cu diabet de tip 2. Pacienții care nu au fost supuși tratamentului sau alți agenți antihiperglicemici au intrat într-o perioadă de tratament de până la 12 săptămâni cu monoterapie cu monformină (doză de 1500 ¥ 1500 mg pe zi) care a inclus spălarea medicamentelor, altele decât metformină, dacă aplicabil. După perioada de rodaj, cei cu control glicemic inadecvat (A1C 6,5% - 10%) au fost randomizați 1: 1 la adăugarea de sitagliptin 100 mg o dată pe zi sau glipizidă timp de 52 de săptămâni. Pacienților cărora li s-a administrat glipizidă li s-a administrat o doză inițială de 5 mg / zi și apoi au fost titrați electiv în următoarele 18 săptămâni la o doză maximă de 20 mg / zi, după cum este necesar pentru a optimiza controlul glicemic. După aceea, doza de glipizidă a trebuit să fie menținută constantă, cu excepția titrării în jos pentru a preveni hipoglicemia. Doza medie de glipizidă după perioada de titrare a fost de 10 mg.
După 52 de săptămâni, sitagliptin și glipizidă au avut reduceri medii similare față de valoarea inițială în A1C în analiza intenției de a trata (Tabelul 6). Aceste rezultate au fost în concordanță cu analiza pe protocol (Figura 2). O concluzie în favoarea non-inferiorității sitagliptinei față de glipizidă poate fi limitată la pacienții cu valori inițiale A1C comparabil cu cele incluse în studiu (peste 70% dintre pacienți au prezentat valori inițiale A1C <8% și peste 90% au avut A1C <9%).
Tabelul 6: Parametrii glicemici într-un studiu de 52 de săptămâni care compară Sitagliptin cu Glipizidă ca terapie suplimentară la pacienții controlați necorespunzător pe Metformin (populație cu intenție de a trata) *
| Sitagliptin 100 mg + Metformin |
glipizide + Metformin |
|
| ||
| A1C (%) | N = 576 | N = 559 |
| Linie de bază (medie) | 7.7 | 7.6 |
| Modificarea de la linia de bază (media ajustată†) | -0.5 | -0.6 |
| FPG (mg / dL) | N = 583 | N = 568 |
| Linie de bază (medie) | 166 | 164 |
| Modificarea de la linia de bază (media ajustată†) | -8 | -8 |
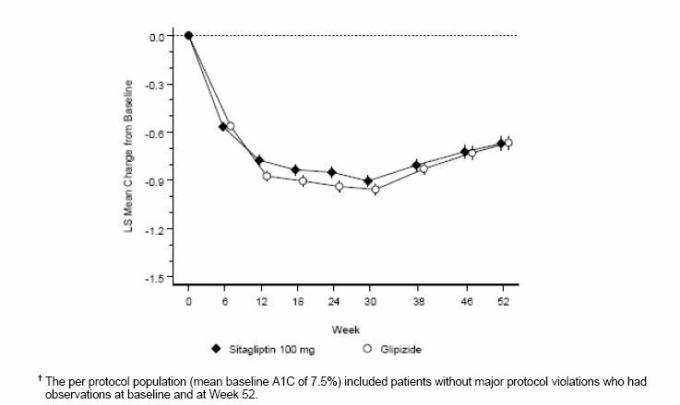
Figura 2: Modificarea medie de la valoarea inițială pentru A1C (%) peste 52 de săptămâni într-un studiu care a comparat Sitagliptin cu Glipizida ca terapie suplimentară la pacienți controlată în mod inadecvat cu metformină (pe populația de protocol) â€
Incidența hipoglicemiei în grupul sitagliptin (4,9%) a fost semnificativ (p <0,001) mai mică decât cea din grupul glipizidelor (32,0%). Pacienții tratati cu sitagliptin au prezentat o scădere semnificativă medie de la nivelul inițial al greutății corporale, comparativ cu o creștere semnificativă în greutate la pacienții administrați glipizidă (-1,5 kg vs. +1,1 kg).
top
Cât este furnizat
Nr. 6747 - Tablete Janumet, 50 mg / 500 mg, sunt comprimate acoperite cu peliculă, roz-deschis, în formă de capsulă, cu "575" decupate pe o parte. Sunt furnizate după cum urmează:
NDC 0006-0575-61 unități de utilizare flacoane de 60
NDC 0006-0575-62 sticle de 180 de unități de utilizare
NDC 0006-0575-52 pachete de 50 blister doză unitară
NDC 0006-0575-82 sticle în vrac de 1000.
Nr. 6749 - Tablete Janumet, 50 mg / 1000 mg, sunt comprimate acoperite cu peliculă roșie, în formă de capsulă, cu "577" decupate pe o parte. Sunt furnizate după cum urmează:
NDC 0006-0577-61 unități de utilizare flacoane de 60
NDC 0006-0577-62 sticle de 180 de unități de utilizare
NDC 0006-0577-52 pachete de 50 blister doză unitară de 50
NDC 0006-0577-82 sticle în vrac de 1000.
A se păstra la 20-25 ° C (68-77 ° F), excursii permise la 15-30 ° C (59-86 ° F).
top
Informații despre consilierea pacientului
Instrucțiuni
Pacienții trebuie informați despre riscurile și beneficiile potențiale ale Janumet și despre modurile alternative de terapie. De asemenea, aceștia trebuie informați despre importanța respectării instrucțiunilor dietetice, a activității fizice regulate, a sângelui periodic monitorizarea glucozei și testarea A1C, recunoașterea și gestionarea hipoglicemiei și hiperglicemiei și evaluarea diabetului complicații. În perioadele de stres, cum ar fi febră, traume, infecții sau intervenții chirurgicale, cerințele de medicamente se pot schimba, iar pacienții trebuie sfătuiți să solicite imediat sfaturi medicale.
Riscurile acidozei lactice datorate componentei metforminei, simptomelor și condițiilor care predispun la dezvoltarea acesteia, așa cum s-a menționat în Avertismente și precauții, trebuie explicat pacienților. Pacienții trebuie sfătuiți să întrerupă imediat Janumet și să anunțe imediat medicul medical dacă există hiperventilație inexplicabilă, mialgie, stare de rău, somnolență neobișnuită, amețeli, bătăi cardiace lente sau neregulate, senzație de senzație de răceală (în special la extremități) sau alte simptome nespecifice apar. Simptomele gastro-intestinale sunt frecvente în timpul inițierii tratamentului cu metformină și pot apărea în timpul inițierii terapiei cu Janumet; cu toate acestea, pacienții ar trebui să se consulte cu medicul lor dacă prezintă simptome inexplicabile. Deși simptomele gastro-intestinale care apar după stabilizare sunt puțin probabil să fie legate de medicamente, un astfel de apariția simptomelor trebuie evaluată pentru a determina dacă aceasta se poate datora acidozei lactice sau a altor grave boală.
Pacienții trebuie sfătuiți împotriva consumului excesiv de alcool, acut sau cronic, în timp ce primesc Janumet.
Pacienții trebuie informați despre importanța testării periodice a funcției renale și a parametrilor hematologici atunci când primesc tratament cu Janumet.
Pacienții trebuie informați că au fost raportate reacții alergice în timpul utilizării post-comercializare a sitagliptinei, una dintre componentele Janumet. Dacă apar simptome ale reacțiilor alergice (inclusiv erupții cutanate, urticarie și umflare a feței, buzelor, limbii și gâtului, apar dificultăți de respirație sau înghițire), pacienții trebuie să înceteze să ia Janumet și să solicite sfaturi medicale prompt.
Medicii trebuie să instruiască pacienții să citească Pachetul Pachetului Introducere înainte de a începe terapia cu Janumet și să recitească de fiecare dată când reînnoirea rețetei. Pacienții trebuie instruiți să informeze medicul sau farmacistul dacă dezvoltă vreun simptom neobișnuit sau dacă vreun simptom cunoscut persistă sau se agravează.
Teste de laborator
Răspunsul la toate terapiile diabetice trebuie monitorizat prin măsurători periodice ale nivelului de glucoză din sânge și A1C, cu scopul de a scădea aceste niveluri către intervalul normal. A1C este util în special pentru evaluarea controlului glicemic pe termen lung.
Monitorizarea inițială și periodică a parametrilor hematologici (de exemplu, hemoglobină / hematocrit și sânge roșu indicii celulari) și funcția renală (creatinină serică) ar trebui să fie efectuate, cel puțin anual. În timp ce anemia megaloblastică a fost rareori observată cu terapia cu metformină, dacă se suspectează acest lucru, deficitul de vitamina B12 trebuie exclus.
Distribuit de:
MERCK & CO., INC., Whitehouse Station, NJ 08889, SUA
9794108
Brevetul SUA nr.: 6.699.871
1 Marcă înregistrată a MERCK & CO., Inc., Whitehouse Station, New Jersey 08889 SUA
2 Marca comercială a MERCK & CO., Inc., Whitehouse Station, New Jersey 08889 SUA
3GLUCOPHAGE® este o marcă înregistrată a Merck Sante S.A.S, un asociat al Merck KGaA din Darmstadt, Germania.
Licențiat companiei Bristol-Myers Squibb.
COPYRIGHT © 2007, 2008 MERCK & CO., Inc.
Toate drepturile rezervate
Etichetarea pacientului aprobat de FDA
Informații pentru pacient
Janumet® (JAN-you-met)
(HCl sitagliptin / metformin)
Tablete
Citiți informațiile despre pacient care vin cu Janumet1 înainte de a începe să o luați și de fiecare dată când primiți o reumplere. Pot exista informații noi. Acest prospect nu ia locul de a discuta cu medicul despre starea sau tratamentul dumneavoastră medical.
Care sunt cele mai importante informații pe care ar trebui să le cunosc despre Janumet?
Clorhidratul de metformină, unul dintre ingredientele din Janumet, poate provoca un efect secundar rar, dar grav, numit acidoză lactică (acumularea acidului lactic în sânge) care poate provoca moartea. Acidoza lactică este o urgență medicală și trebuie tratată într-un spital.
Încetați să luați Janumet și sunați imediat medicul dumneavoastră dacă aveți oricare dintre următoarele simptome ale acidozei lactice:
- Te simți foarte slab și obosit.
- Aveți dureri musculare neobișnuite (nu normale).
- Ai probleme cu respirația.
- Aveți probleme stomacale sau intestinale inexplicabile cu greață și vărsături sau diaree.
- Simțiți frig, mai ales în brațe și picioare.
- Vă simțiți amețit sau cu capul.
- Ai un ritm cardiac lent sau neregulat.
Aveți o șansă mai mare de a obține acidoză lactică dacă:
- au probleme renale.
- au probleme cu ficatul.
- au insuficiență cardiacă congestivă care necesită tratament cu medicamente.
- bea mult alcool (foarte des sau băutură „cu chef” pe termen scurt).
- se deshidratează (pierde o cantitate mare de lichide ale corpului). Acest lucru se poate întâmpla dacă sunteți bolnav de febră, vărsături sau diaree. Deshidratarea se poate întâmpla și atunci când transpirați mult cu activitate sau exerciții fizice și nu beți suficiente lichide.
- au anumite teste cu raze X cu coloranți injectabili sau agenți de contrast.
- au operatie.
- au un atac de cord, o infecție severă sau un AVC.
- au 80 de ani sau mai mult și nu v-au testat funcția renală.
Ce este Janumet?
Tabletele Janumet conțin două medicamente eliberate pe bază de rețetă, sitagliptin (JANUVIA ™ 2) și metformin. Janumet poate fi utilizat împreună cu dieta și exercițiile fizice pentru a scădea glicemia la pacienții adulți cu diabet de tip 2. Medicul dumneavoastră va stabili dacă Janumet este potrivit pentru dvs. și va stabili cel mai bun mod de a începe și de a continua tratamentul diabetului.
Janumet:
- ajută la îmbunătățirea nivelului de insulină după masă.
- ajută organismul să răspundă mai bine la insulina pe care o face în mod natural.
- scade cantitatea de zahăr făcută de organism.
- este puțin probabil să provoace glicemie scăzută (hipoglicemie) atunci când este luat de la sine pentru a trata glicemia mare.
Janumet nu a fost studiat la copii sub 18 ani.
Janumet nu a fost studiat cu insulină, un medicament cunoscut că cauzează un nivel scăzut de zahăr din sânge.
Cine nu ar trebui să ia Janumet?
Nu luați Janumet dacă:
- au diabet de tip 1.
- au anumite probleme renale.
- au afecțiuni numite acidoză metabolică sau cetoacidoză diabetică (cetone crescute în sânge sau urină).
- au avut o reacție alergică la Janumet sau sitagliptin (JANUVIA), una dintre componentele Janumet.
- urmează să primească o injecție de coloranți sau agenți de contrast pentru o procedură cu raze X, Janumet va trebui oprită pentru o perioadă scurtă de timp. Discutați cu medicul dumneavoastră când să opriți Janumet și când să începeți din nou. Vezi "Care este cea mai importantă informație pe care ar trebui să o știu despre Janumet?"
Ce trebuie să-i spun medicului meu înainte și în timpul tratamentului cu Janumet?
Este posibil ca Janumet să nu fie potrivit pentru tine. Spuneți medicului dumneavoastră toate condițiile medicale, inclusiv dacă:
- au probleme renale.
- au probleme cu ficatul.
- au avut o reacție alergică la Janumet sau sitagliptin (JANUVIA), una dintre componentele Janumet.
- au probleme cardiace, inclusiv insuficiență cardiacă congestivă.
- sunt mai vechi de 80 de ani. Pacienții peste 80 de ani nu trebuie să ia Janumet decât dacă este verificată funcția renală și este normală.
- bea mult alcool (băutul tot timpul sau băutură „cu chef” pe termen scurt).
- sunt însărcinate sau intenționează să rămână însărcinate. Nu se știe dacă Janumet îți va dăuna copilului nenăscut. Dacă sunteți gravidă, discutați cu medicul dumneavoastră despre cea mai bună modalitate de a vă controla glicemia în timp ce sunteți gravidă. Dacă utilizați Janumet în timpul sarcinii, discutați cu medicul dumneavoastră despre cum puteți fi în registrul Janumet. Numărul de telefon gratuit pentru registrul de sarcină este 1-800-986-8999.
- alăptează sau intenționează să alăpteze. Nu se știe dacă Janumet va trece în laptele matern. Discutați cu medicul dumneavoastră despre cea mai bună metodă de a vă hrăni copilul dacă luați Janumet.
Spuneți medicului dumneavoastră despre toate medicamentele pe care le luați, inclusiv medicamentele fără prescripție medicală și fără prescripție medicală, vitamine și suplimente pe bază de plante. Janumet poate afecta cât de bine funcționează alte medicamente și unele medicamente pot afecta cât de bine funcționează Janumet.
Cunoașteți medicamentele pe care le luați. Păstrați o listă cu medicamentele dvs. și arătați-o medicului și farmacistului când primiți un medicament nou. Discutați cu medicul dumneavoastră înainte de a începe orice medicament nou.
Cum ar trebui să iau Janumet?
- Medicul dumneavoastră vă va spune câte tablete Janumet trebuie să luați și cât de des trebuie să le luați. Luați Janumet exact așa cum vă spune medicul dumneavoastră.
- Este posibil ca medicul dumneavoastră să fie necesar să vă crească doza pentru a vă controla glicemia.
- Medicul dumneavoastră vă poate prescrie Janumet împreună cu o sulfonilurea (un alt medicament pentru scăderea glicemiei). Vedeți "Care sunt efectele secundare posibile ale Janumet?" pentru informații despre riscul crescut de glicemie scăzută.
- Luați Janumet cu mese pentru a vă scădea șansa de stomac supărat.
- Continuați să luați Janumet atât timp cât vă spune medicul.
- Dacă luați prea mult Janumet, apelați imediat medicul sau centrul de control al otrăvurilor.
- Dacă vă lipsește o doză, luați-o cu mâncare imediat ce vă amintiți. Dacă nu vă amintiți până când este timpul pentru următoarea doză, săriți doza pierdută și să reveniți la programul dvs. obișnuit. Nu luați două doze de Janumet în același timp.
- Este posibil să fie nevoie să nu mai luați Janumet pentru o perioadă scurtă de timp. Apelați medicul pentru instrucțiuni dacă:
- sunt deshidratate (au pierdut prea mult lichid corporal). Deshidratarea poate apărea dacă sunteți bolnav cu vărsături severe, diaree sau febră sau dacă beți mult mai puțin lichid decât în mod normal.
- intenționează să faci o intervenție chirurgicală.
- urmează să primească o injecție de colorant sau agent de contrast pentru o procedură cu raze X.
Vezi "Care este cea mai importantă informație pe care ar trebui să o știu despre Janumet?" și "Cine nu ar trebui să ia Janumet?"
- Atunci când corpul tău este supus unor tipuri de stres, cum ar fi febra, traumele (cum ar fi un accident de mașină), infecția sau intervenția chirurgicală, cantitatea de medicament pentru diabet de care aveți nevoie se poate schimba. Spuneți imediat medicului dumneavoastră dacă aveți oricare dintre aceste afecțiuni și urmați instrucțiunile medicului dumneavoastră.
- Monitorizează-ți glicemia după cum îți spune medicul.
- Rămâneți pe dieta prescrisă și programul de exerciții fizice în timp ce luați Janumet.
- Discutați cu medicul dumneavoastră despre cum să preveniți, să recunoașteți și să gestionați glicemia scăzută (hipoglicemie), zahărul ridicat în sânge (hiperglicemie) și complicațiile diabetului.
- Medicul vă va monitoriza diabetul cu teste de sânge obișnuite, inclusiv nivelul glicemiei și hemoglobina A1C.
- Medicul dumneavoastră va face analize de sânge pentru a vă verifica funcția renală înainte și în timpul tratamentului cu Janumet.
Care sunt efectele secundare posibile ale Janumet?
Janumet poate provoca reacții adverse grave. Vezi "Care este cea mai importantă informație pe care ar trebui să o știu despre Janumet?"
Reacțiile adverse frecvente când luați Janumet includ:
- nasul înfundat sau curgător și dureri în gât
- infecție respiratorie superioara
- diaree
- greață și vărsături
- gaze, disconfort stomacal, indigestie
- slăbiciune
- durere de cap
Luând Janumet cu mese poate ajuta la reducerea reacțiilor adverse frecvente ale stomacului metforminei care apar de obicei la începutul tratamentului. Dacă aveți probleme de stomac neobișnuite sau neașteptate, discutați cu medicul dumneavoastră. Problemele de stomac care încep mai târziu în timpul tratamentului pot fi un semn de ceva mai grav.
Anumite medicamente pentru diabet, cum ar fi sulfonilureele și meglitinidele, pot provoca un nivel scăzut de zahăr din sânge (hipoglicemie). Când Janumet este utilizat cu aceste medicamente, este posibil să aveți zaharuri din sânge prea mici. Medicul dumneavoastră vă poate prescrie doze mai mici de medicamente sulfoniluree sau meglitinide. Spuneți medicului dumneavoastră dacă aveți probleme cu glicemia scăzută.
Următoarele reacții adverse suplimentare au fost raportate în general la Janumet sau sitagliptin:
- Reacții alergice grave se pot întâmpla cu Janumet sau sitagliptin, unul dintre medicamentele din Janumet. Simptomele unei reacții alergice grave pot include erupții cutanate, urticarie și umflarea feței, buzelor, limbii și gâtului, dificultăți de respirație sau de înghițire. Dacă aveți o reacție alergică, încetați să luați Janumet și sunați imediat medicul. Medicul dumneavoastră vă poate prescrie un medicament pentru a vă trata reacția alergică și un medicament diferit pentru diabetul dumneavoastră.
- Enzime hepatice crescute.
- Inflamarea pancreasului.
Acestea nu sunt toate efectele secundare posibile ale Janumet. Pentru mai multe informații, adresați-vă medicului dumneavoastră.
Spuneți medicului dumneavoastră dacă aveți vreun efect secundar care vă deranjează, este neobișnuit sau nu dispărește.
Cum ar trebui să păstrez Janumet?
A se păstra Janumet la temperatura camerei, la 20-25 ° C.
Păstrați Janumet și toate medicamentele la îndemâna copiilor.
Informații generale despre utilizarea Janumet
Medicamentele sunt uneori prescrise pentru afecțiuni care nu sunt menționate în prospectele de informare a pacienților. Nu folosiți Janumet pentru o afecțiune pentru care nu a fost prescris. Nu dați Janumet altor persoane, chiar dacă au aceleași simptome pe care le aveți. Le poate dăuna.
Acest prospect rezumă cele mai importante informații despre Janumet. Dacă doriți să aflați mai multe informații, discutați cu medicul dumneavoastră. Puteți solicita medicului sau farmacistului informații despre Janumet care sunt scrise pentru profesioniștii din sănătate. Pentru mai multe informații sunați la 1-800-622-4477.
Care sunt ingredientele din Janumet?
Ingrediente active: sitagliptin și clorhidrat de metformină.
Ingrediente inactive: celuloză microcristalină, polivinilpirolidonă, lauril sulfat de sodiu și stearil fumarat de sodiu. Acoperirea cu film de tabletă conține următoarele ingrediente inactive: alcool polivinilic, polietilenglicol, talc, dioxid de titan, oxid roșu de fier și oxid de fier negru.
Ce este diabetul de tip 2?
Diabetul de tip 2 este o afecțiune în care corpul tău nu produce suficientă insulină, iar insulina pe care corpul tău o produce nu funcționează la fel de bine. De asemenea, corpul tău poate face prea mult zahăr. Când se întâmplă acest lucru, zahărul (glucoza) se acumulează în sânge. Acest lucru poate duce la probleme medicale grave.
Principalul obiectiv al tratamentului diabetului este de a reduce nivelul glicemiei la un nivel normal. Scăderea și controlul zahărului din sânge poate ajuta la prevenirea sau întârzierea complicațiilor diabetului, cum ar fi probleme cardiace, probleme renale, orbire și amputație.
Glicemia ridicată poate fi scăzută prin dietă și exerciții fizice, precum și prin anumite medicamente, atunci când este necesar.
Eliberat în martie 2009
Distribuit de:
MERCK & CO., INC., Whitehouse Station, NJ 08889, SUA
Ultima actualizare: 03/09
Janumet, Sitagliptin și Metformin Clorhidrat, Informații despre pacient (în engleză simplă)
Informații detaliate despre semne, simptome, cauze, tratamente ale diabetului
Informațiile din această monografie nu sunt destinate să acopere toate utilizările, indicațiile, precauțiile, interacțiunile medicamentoase sau efectele adverse posibile. Aceste informații sunt generalizate și nu sunt destinate unor sfaturi medicale specifice. Dacă aveți întrebări despre medicamentele pe care le luați sau doriți mai multe informații, consultați medicul, farmacistul sau asistenta medicală.
înapoi la: Căutați toate medicamentele pentru diabet



